Cos’è e perché conta
Il Milli-Spinner è un dispositivo per trombectomia endovascolare sviluppato alla Stanford University che riduce il volume del trombo comprimendone e compattandone la rete di fibrina, senza frammentarlo. In modelli preclinici ha più che raddoppiato l’efficacia rispetto ai sistemi correnti e ha riportato ricanalizzazione rapida in scenari simulati di ictus ischemico e embolia polmonare.
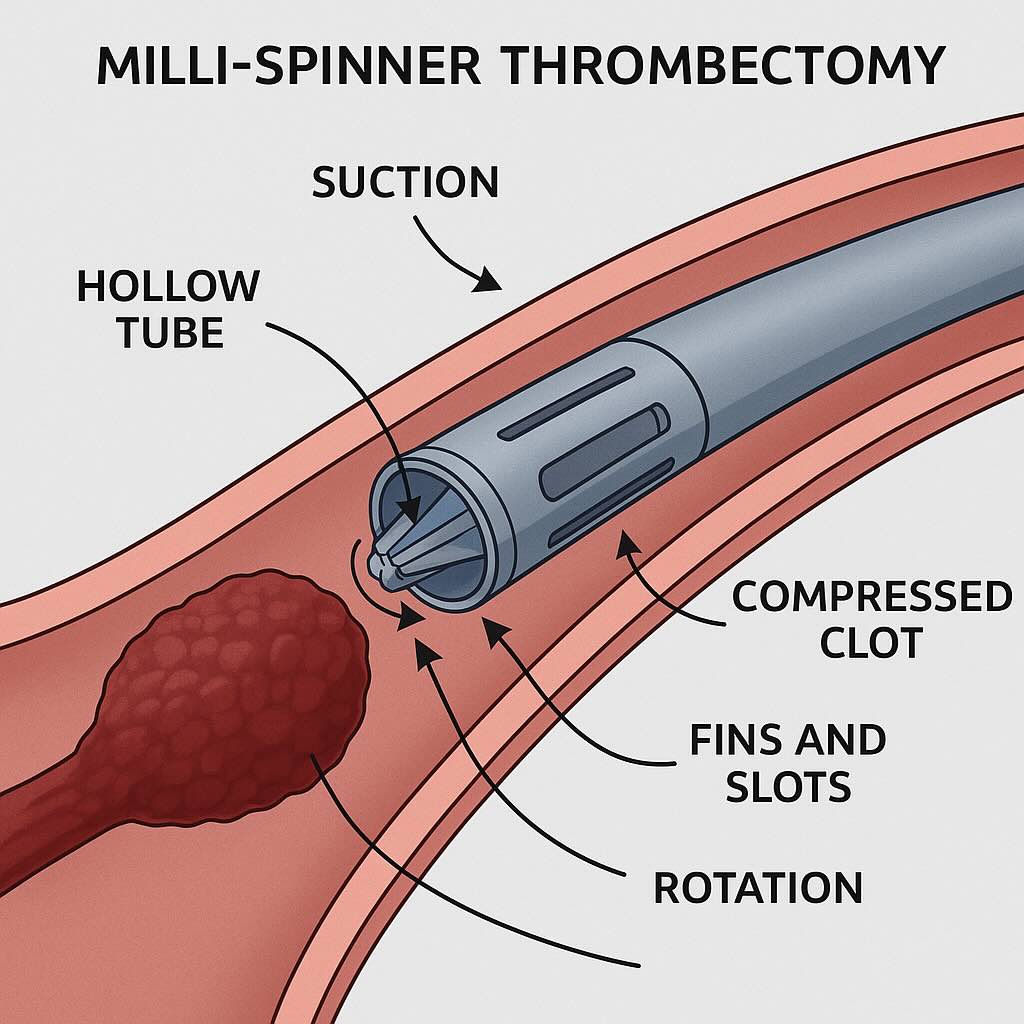
Come funziona (compressione + taglio, non “tritare”)
Il dispositivo è un tubo cavo che ruota ad alta velocità; un disegno con alette e fessure crea una suzione localizzata che spinge il coagulo contro la punta, mentre la rotazione applica compressione e shear: i globuli rossi vengono “spremuti” fuori dalla matrice e la fibrina si addensa in una sfera compatta rimovibile. Riduzione volumetrica fino al 95% (Nature).
Prestazioni misurate (tempi e percentuali)
Nei test: rimozione del trombo in ~45 s nel modello di embolia polmonare; ripristino del flusso cerebrale in ~8 s in un modello di ictus; suino in vivo: rimozione in un’unica manovra dopo ~2 min di “debulking”; ricanalizzazione completa >80% con trombi ricchi di fibrina. L’articolo accademico riporta riduzioni fino al 95%, mentre il preprint cita fino al 90%, a seconda della composizione del coagulo.
Perché è diverso dagli attuali cateteri
Aspirazione e stent retriever spesso rompono il coagulo (fino a fallimenti 10–30% e primo-passaggio ~50%), con rischio di emboli distali. Il Milli-Spinner invece rimodella il trombo e ne riduce la dimensione prima della rimozione, migliorando il tasso di successo al primo tentativo—fino al 90% perfino con i coaguli più “duri”, secondo Stanford.
Produzione additiva: dove entra la stampa 3D
I prototipi sono stati stampati in 3D: versione da 2,5 mm con Formlabs Form 3+ e resina Grey; versioni radio-opache da 1,5/1,3/1,2 mm realizzate con DLP custom a 385 nm, con resina caricata a solfato di bario e ossido di ferro per visibilità in fluoroscopia. Qui entrano in gioco aziende come Formlabs (macchina e materiale) e i fornitori di pigmenti/radio-opacizzanti.
Farmacologia mirata e possibili estensioni
Il lume cavo può rilasciare farmaci direttamente nel sito (dimostrato con tracciante), con velocità modulabile dalla rotazione; il team sta esplorando l’uso della stessa suzione localizzata per frammenti di calcoli renali.
Stato della ricerca, pubblicazione e trasferimento tecnologico
Il lavoro è pubblicato su Nature (4 giugno 2025) con dati su modelli in vitro e suino; esiste anche un preprint arXiv (luglio 2024). La Stanford OTL indica avanzamenti verso brevetti (WO2025038507) e spin-off supportato dall’HIT Fund dell’università.
Indicazioni cliniche e limiti attuali
Target: ictus ischemico, infarto miocardico, embolia polmonare, trombosi periferica. Ad oggi i dati sono preclinici; gli autori puntano a ottenere l’approvazione clinica “il prima possibile”, ma serviranno trial sull’uomo e valutazioni su sicurezza endoteliale e frammentazione residua.
Dettagli tecnici salienti
-
Geometria: tubo cavo con alette e fessure ottimizzate (CFD).
-
Materiali: resine fotopolimeriche (Grey; miscele caricate BaSO₄/Fe₂O₃ per contrasto).
-
Dimensioni prototipi: 1,2–2,5 mm di diametro.
-
Metodi: SLA (Formlabs) e DLP custom; guida fluoroscopica.