I RICERCATORI DELL’UNIVERSITÀ DEL MINNESOTA UTILIZZANO LA TECNOLOGIA DI MOTION CAPTURE PER STAMPARE I SENSORI 3D DIRETTAMENTE SUGLI ORGANI IN ESPANSIONE
Stampare direttamente sui tessuti molli in movimento è una sfida perché i sensori devono essere in grado di adattarsi ai parametri in costante cambiamento dell’organo. La nuova tecnica del team di ricerca, d’altra parte, supera questo ostacolo utilizzando le doppie fotocamere per creare un percorso utensile per la stampa 3D in tempo reale. Non solo questo metodo potrebbe essere utilizzato dal personale medico per monitorare i pazienti contagiosi a distanza di sicurezza, ma secondo il team di ricerca, potrebbe anche essere applicato per diagnosticare e monitorare i polmoni di coloro che soffrono di COVID-19.
“Stiamo spingendo i confini della stampa 3D in modi che non avevamo nemmeno immaginato anni fa”, ha affermato il professor Michael McAlpine, capo ricercatore del progetto. “In futuro, la stampa 3D non riguarderà solo la stampa, ma farà invece parte di un più ampio sistema robotico autonomo. Questo potrebbe essere importante per malattie come COVID-19, in cui gli operatori sanitari sono a rischio durante il trattamento dei pazienti. “
I recenti progressi nella produzione di additivi hanno ampliato la gamma di materiali di stampa 3D compatibili da materie plastiche e metalli convenzionali per includere conduttori e biomateriali. Nonostante questa progressione, AM ha trovato difficile avere un impatto nelle applicazioni di bioprinting che colpiscono le superfici biologiche vive, perché sono tipicamente morbide e subiscono costante movimento e deformazione. Inoltre, poiché le stampanti 3D si basano su un design prescritto che viene prodotto offline e quindi trasferito sulla superficie biologica, ciò si traduce in una discrepanza e il sistema sta essenzialmente fabbricando “ciechi”.
Anche la regolazione manuale del processo di stampa non è un’opzione praticabile, poiché i processi di trasferimento possono interrompere fragili costrutti 3D come materiali idrogel e portare a costosi errori umani. I ricercatori hanno identificato una soluzione alternativa: la stampa in situ per integrare in modo autonomo i sensori sulla superficie target. Per raggiungere questo obiettivo, era necessaria una nuova intelligenza artificiale a circuito chiuso (AI), al fine di adattare il processo di fabbricazione in tempo reale rilevando dinamicamente gli stati geometrici dei substrati biologici.
Il team di ricerca del Minnesota aveva sviluppato un sistema a circuito chiuso che tracciava il movimento di una mano non deformante nel 2018, ma questo approccio richiederebbe lo sviluppo di un algoritmo complesso in grado di tracciare con precisione i dati di deformazione dimensionale elevata. Invece, i ricercatori hanno proposto che lo spazio di deformazione della superficie target potesse essere “appreso” da un set di dati di scansioni 3D. Ciò consentirebbe il recupero accurato della geometria della superficie in 3D, tramite una serie di marcatori fiduciosi tracciati da un sistema di telecamere stereo e utilizzati per adattare dinamicamente il percorso degli strumenti di stampa 3D in tempo reale.
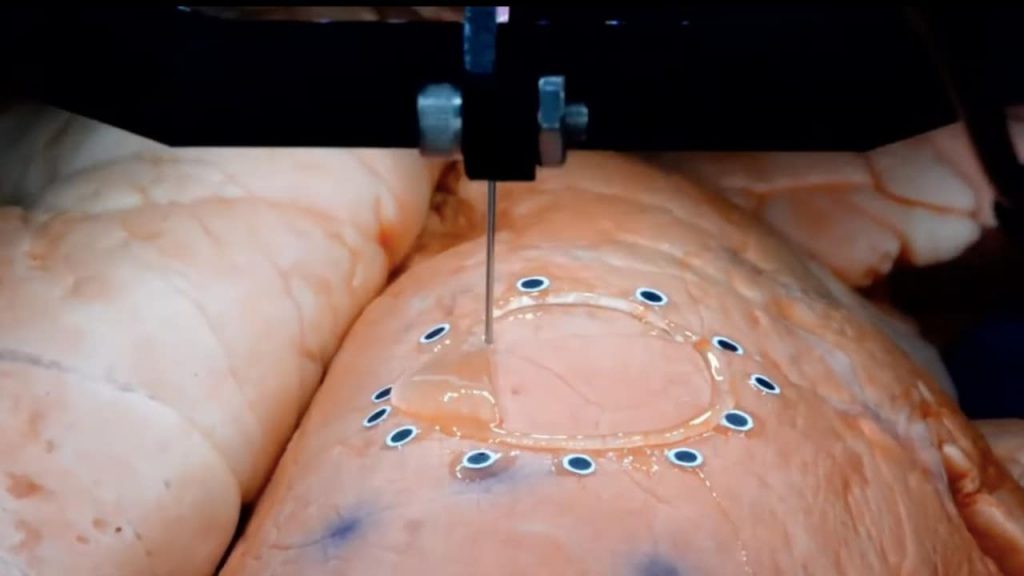
Affinché questo approccio abbia successo, i sensori di deformazione utilizzati per calcolare le misurazioni della deformazione dovevano essere compatibili con la superficie del tessuto polmonare e il processo di stampa 3D in situ. I design convenzionali dei sensori si basano sulla densa confezione di array di sensori, elettrodi e interconnessioni in miniatura per migliorare la risoluzione, ma questo approccio non è compatibile con le incertezze che possono verificarsi durante la stampa. In alternativa, il team di ricerca ha sviluppato un nuovo sensore utilizzando una combinazione di idrogel ionici e sensori di tomografia ad impedenza elettrica (EIT), grazie alla loro elevata trasparenza e elasticità. Per dimostrare il loro nuovo sensore e la tecnica di acquisizione del movimento, i ricercatori hanno stampato in 3D un sensore di deformazione EIT a base di idrogel direttamente su un polmone respiratorio per monitorarne la deformazione.
Mentre i ricercatori avrebbero potuto utilizzare un sistema di telecamere stereo per recuperare la varia geometria 3D della superficie dell’organo in tempo reale, i suoi algoritmi di ricostruzione non sarebbero abbastanza accurati, poiché è necessaria una precisione a livello di submillimetro per evitare lesioni ai tessuti. In alternativa, il team ha ideato una procedura in due fasi in base alla quale il sistema ha appreso un modello parametrico della geometria della superficie, che è stato integrato da una stima dei parametri del polmone utilizzando un set di marker fiduciali.
Nella prima fase, la deformazione superficiale è stata modellata utilizzando il movimento di 12 marker fiduciali e 3968 waypoint che sono stati estratti per creare il percorso utensile di stampa. Prima della proiezione del percorso utensile planare, sono state apportate correzioni in modo da riflettere la crescita fisica delle dimensioni del sensore quando la superficie si espandeva e il restringimento quando la superficie si contraeva. Durante la seconda fase, due telecamere per visione artificiale sono state montate sulla testa di estrusione della stampante 3D per il monitoraggio in tempo reale del processo di rilevamento. Le serie temporali dei parametri riflettevano il sudore polmonare e venivano utilizzate per stimare il percorso utensile conforme variabile nel tempo che era adattivo al movimento del corpo rigido del tessuto.
Dopo che il percorso utensile adattivo è stato trasferito sulla stampante 3D, l’ugello di estrusione ha seguito i profili di velocità di stampa specificati dall’utente e i waypoint ricampionati. L’incorporazione della stima della deformazione ha ridotto l’errore medio della modellazione di forme da 0,3 mm a meno di 0,02 mm e l’errore totale rientrava nella tolleranza di ± 0,8 mm. Inoltre, l’inchiostro a idrogel ionico mostrava un comportamento al diradamento con riduzione della viscosità al di sopra della velocità di taglio di 0,1 s − 1. Questa bassa viscosità ha permesso l’estrusione regolare dell’inchiostro dall’ugello di stampa sotto pressione pneumatica e ne ha migliorato la controllabilità. Dopo il collegamento incrociato con la luce UV, l’inchiostro a idrogel ha anche dimostrato una elasticità simile a quella dei tessuti secondo i risultati dei test di trazione uniassiali.
Il sensore EIT, costituito da uno strato sottile continuo di idrogel ed elettrodi di rame, era incorporato in un anello di silicone morbido che poteva formare legami chimici con l’idrogel, per mantenere interfacce idrogel-elettrodo stabili. Durante il test, sono state prese quaranta misurazioni da coppie di elettrodi adiacenti per una stima completa della mappa della deformazione e l’errore medio massimo registrato è stato del 5,25%, simile a quello della ricostruzione della scansione TC. Al fine di dimostrare la capacità di stampa 3D del loro nuovo sistema in situ basato su AI, i ricercatori hanno fabbricato il sensore di deformazione EIT direttamente su un polmone suino.
Per simulare le deformazioni dell’organo, la trachea del polmone è stata collegata a un regolatore pneumatico digitale e la geometria della superficie sotto ogni stato di deformazione è stata quindi campionata da uno scanner a luce strutturata. Usando un sistema di cavalletto di stampa 3D personalizzato, gli elettrodi incorporati in un anello di silicone sono stati quindi fissati allo strato stampato ed esposti alla luce UV per il reticolazione. La mappatura spaziale dei polmoni è stata stimata e visualizzata in tempo reale, che ha catturato con successo la contrazione ciclica dell’organo. Non solo i sensori sono stati in grado di aderire alla superficie polmonare sotto una deformazione ripetitiva, ma potevano essere rimossi sommariamente senza danni ai tessuti o lasciando residui.
Di conseguenza, il team di ricerca ha dimostrato con successo il monitoraggio in situ della deformazione degli organi, con un sensore morbido che è stato stampato in 3D in vitro su un polmone respiratorio. Il nuovo metodo ha integrato l’apprendimento automatico offline con il monitoraggio online basato sulla visione computerizzata e un inchiostro conduttore idrogel con una configurazione di rilevamento EIT, per ottenere questo risultato. Sebbene il team abbia riconosciuto che la biocompatibilità dei sensori potrebbe essere migliorata, la precisione del metodo è migliorata, suggeriscono che potrebbe aprire nuove applicazioni chirurgiche per la bioprinting. Ad esempio, in scenari clinici in cui sono richieste iniezioni di materiali biologici come colla chirurgica e innesti cutanei, la stampa 3D autonoma in situ potrebbe sostituire il funzionamento manuale, per ottenere un controllo spaziale preciso su durate più lunghe.