GLI SCIENZIATI SVILUPPANO UNA NUOVA TECNICA DI BIOPRINTING 3D A RISOLUZIONE SINGOLA ULTRA PRECISA
I ricercatori dell’Università di scienze applicate di Monaco hanno sviluppato un approccio di bioprinting 3D altamente accurato in grado di creare tessuti umani con una risoluzione di una singola cellula.
Sparando un laser ultra corto Near Infrared (NIR) in un idrogel posizionato appena sotto uno strato di cellule, il team è stato in grado di espellere minuscoli ammassi cellulari e impacchettarli in uno scaffold 3D. Il nuovo processo consente il trasferimento di singole cellule in base alla loro morfologia con una vitalità del 93-99% e, con un’ulteriore automazione, gli scienziati ritengono che potrebbe produrre trapianti di tessuto funzionale.
All’interno dei circoli scientifici, il potenziale dei sostituti dei tessuti molli bioprintati è ben noto e molto sperimentato, in particolare quando si tratta di ricerca e sviluppo di farmaci e prevenzione della degenerazione cellulare legata all’età. Nonostante ciò, e il fatto che negli ultimi anni siano stati sviluppati molti approcci diversi alla creazione di scaffold tissutali, il posizionamento preciso delle singole cellule rimane una sfida significativa.
Sebbene gli approcci basati su getto d’inchiostro e drop-on-demand abbiano già dimostrato la precisione di una singola cella, spesso soffrono sia di bassa precisione che di redditività. In alternativa, le tecniche di modellazione delle celle acustiche si sono dimostrate meno dannose e hanno raggiunto alti livelli di risoluzione, ma questi metodi non consentono la manipolazione di cellule specifiche.
Dato il potenziale del controllo puntuale di una singola cellula nell’incoraggiare la proliferazione e, infine, progettare tessuti molli umani funzionali e su misura, gli scienziati hanno sviluppato il loro nuovo approccio nel 2018. Basato su un laser NIR pulsante, la tecnica del team ha permesso loro di trasferire piccole goccioline di idrogel di circa 10-30 cellule su un substrato bersaglio.
Nella loro ultima ricerca, gli scienziati di Monaco hanno ora perfezionato questa procedura, per consentire la selezione di cellule specifiche da un serbatoio, prima di spostarle su una superficie bersaglio. Con un alto livello di accuratezza, risoluzione e sopravvivenza cellulare, la tecnica rivista dei ricercatori potrebbe rappresentare un passo significativo verso trapianti di tessuto più praticabili.
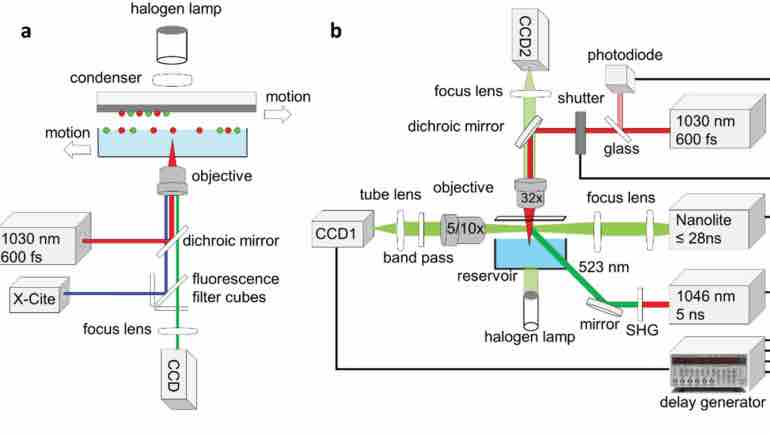
Nell’ambito dell’approccio ottimizzato dei ricercatori, hanno montato la loro configurazione originale su un microscopio ottico invertito, sul quale potevano identificare le cellule in base alla loro forma, dimensione o fluorescenza. Un laser da 1030 nm è stato quindi sparato nell’idrogel sottostante, a una lunghezza d’onda sufficiente a far “proiettare” le cellule in gruppi singoli o multipli, senza danneggiare la loro vitalità complessiva.
Durante i test, gli scienziati hanno stampato file di cellule staminali mesenchimali umane (hMSC) con spazi di 50, 100 e 200 µm su un substrato rivestito di gelatina. Dopo un’analisi dettagliata, i risultati hanno mostrato che il team aveva raggiunto un livello estremamente elevato di accuratezza, con la maggior parte delle cellule che deviavano dalla loro posizione target di meno di un diametro di cella (14-32 µm).
Per valutare l’impatto della loro tecnica sulla vitalità delle hMSC, i ricercatori le hanno poi depositate su una superficie carica di collagene, ottenendo una sopravvivenza fino al 100%. Tuttavia, le cellule distanziate a una distanza di 200 µm si sono effettivamente allontanate l’una dall’altra, suggerendo che i loro segnali meccanici non potevano raggiungere le cellule vicine.
Inoltre, è stato riscontrato che il trasferimento manuale di hMSC richiede circa 20 secondi per cella, limitando la scalabilità del processo. Al fine di aumentare le velocità di trasferimento cellulare, gli scienziati ritengono che in futuro potrebbe essere possibile combinare il loro processo con la stereolitografia a due fotoni (2PP), consentendo la creazione di nuovi dispositivi organo su chip e, infine, funzionali sostituti dei tessuti umani.
Approcci misti di bioprinting
La bioprinting rimane una tecnologia sperimentale ma in rapido progresso e, di conseguenza, sono attualmente in fase di sviluppo una varietà di approcci di deposizione cellulare.
I ricercatori dell’Università di Bath e dell’Università di Bristol hanno sviluppato una nuova tecnica di bioprinting di energia acustica chiamata “sonolitografia”. Il nuovo processo del team, che utilizza le onde ultrasoniche per depositare con precisione i modelli di particelle su un substrato, potrebbe essere implementato in futuro all’interno di applicazioni di test antidroga.
Gli scienziati dell’Università di Buffalo hanno adottato un approccio completamente diverso, ideando un rapido processo di bioprinting 3D basato su SLA . Utilizzando la loro tecnica, i ricercatori sono stati in grado di ridurre il tempo necessario per creare strutture di idrogel cariche di cellule, da oltre sei ore a soli diciannove minuti.
Al contrario, ricercatori come quelli dell’Università di Montreal , hanno recentemente cercato di adottare laser a bassa energia come mezzo per sviluppare nuovi metodi di bioprinting 3D “drop-on-demand” . In generale, l’approccio del team prevede il getto di cellule una sull’altra per formare goccioline più grandi, che potrebbero essere utilizzate per costruire futuri tessuti molli.
I risultati dei ricercatori sono dettagliati nel loro documento intitolato ” Bioprinting a cellula singola con impulsi laser ultracorti “. La ricerca è stata co-autrice di Jun Zhang, Patrick Byers, Amelie Erben, Christine Frank, Levin Schulte ‐ Spechtel, Michael Heymann, Denitsa Docheva, Heinz P. Huber, Stefanie Sudhop e Hauke Clausen ‐ Schaumann.