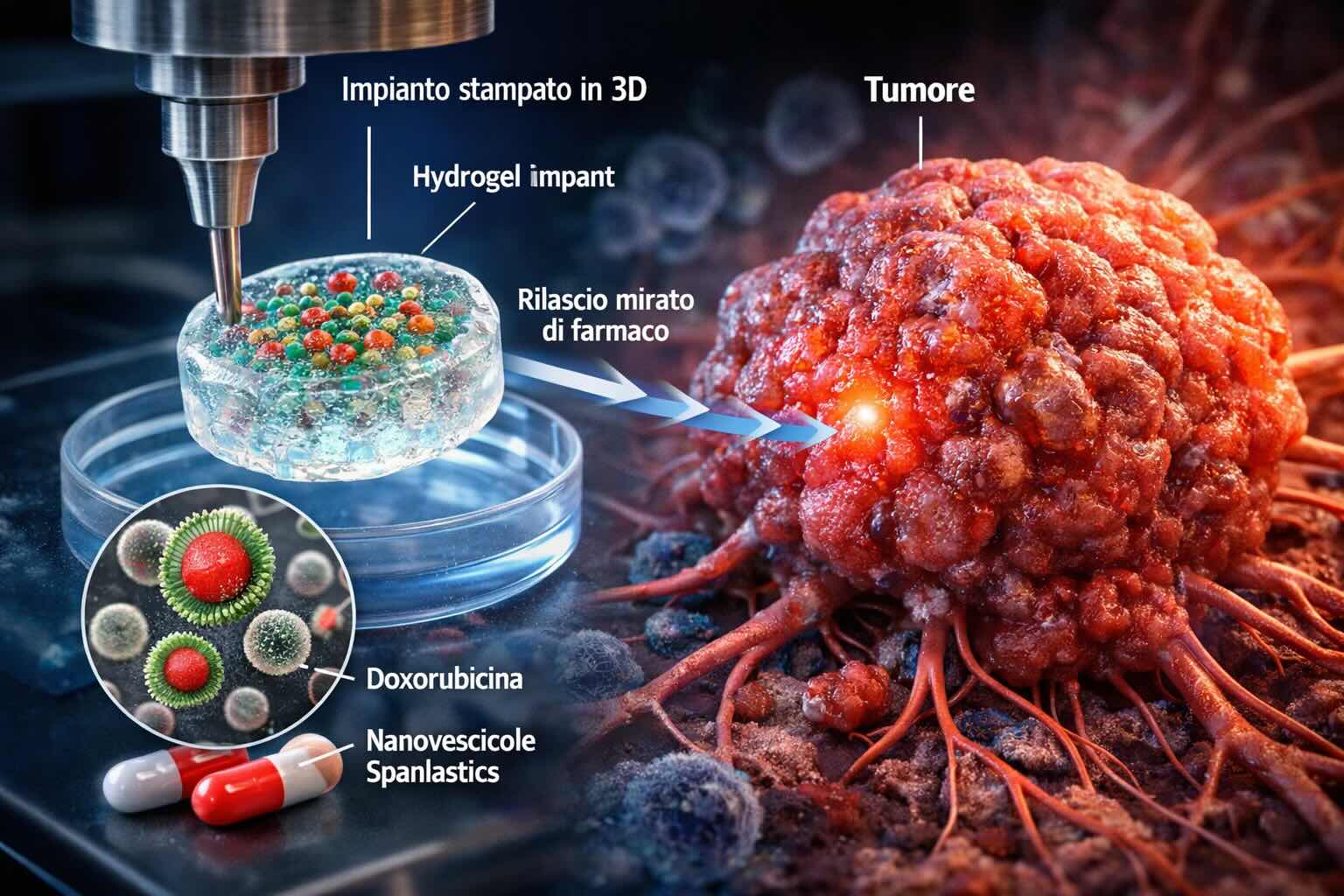
Impianti in idrogel stampati in 3D per rilasciare farmaci antitumorali direttamente sul tumore
Un impianto stampato in 3D per portare la chemioterapia dove serve
Un gruppo di ricerca della University of Mississippi, attraverso la School of Pharmacy e il dipartimento di Pharmaceutics and Drug Delivery, ha sviluppato un sistema sperimentale che punta a rilasciare farmaci antitumorali direttamente in prossimità del tumore invece di disperderli in tutto l’organismo. Il lavoro, firmato tra gli altri da Elom Doe, Abigail Alabi, Leela Raghava Jaidev Chakka e Mohammed Maniruzzaman, è stato pubblicato sulla rivista Pharmaceutical Research. Nelle fonti primarie consultate non compaiono partner industriali indicati come co-sviluppatori del progetto: il lavoro emerge come ricerca accademica, pubblicata da Springer Nature.
Come funziona il sistema di rilascio locale
La piattaforma combina due elementi. Il primo è un impianto morbido in idrogel di alginato, realizzato con stampa 3D. Il secondo è un insieme di nanovescicole elastiche chiamate spanlastics, caricate con doxorubicina, un chemioterapico molto usato ma noto per la sua tossicità sistemica. Nel lavoro sperimentale, queste nanovescicole vengono incorporate nella matrice stampata in 3D così da creare un piccolo deposito locale capace di rilasciare il farmaco in modo prolungato. L’obiettivo è concentrare la terapia nella zona del tumore e ridurre l’esposizione dei tessuti sani.
Perché gli spanlastics sono al centro della ricerca
Gli spanlastics sono vescicole nanometriche deformabili basate su tensioattivi non ionici. La letteratura li descrive come vettori promettenti perché possono migliorare il trasporto del principio attivo, aumentarne la biodisponibilità e contribuire a ridurne la tossicità rispetto a sistemi di somministrazione meno selettivi. Nel lavoro della University of Mississippi questa logica viene portata in un impianto locale: le nanovescicole non sono solo un contenitore del farmaco, ma diventano parte di una struttura stampata che funge da deposito terapeutico.
Il ruolo della tecnica FRESH e dell’idrogel di alginato
Per fabbricare questi impianti, il team usa il metodo FRESH, acronimo di Freeform Reversible Embedding of Suspended Hydrogels. Questa tecnica di biostampa è stata sviluppata per permettere la deposizione precisa di idrogel molto morbidi dentro un bagno di supporto reversibile, così da ottenere strutture che con metodi convenzionali sarebbero difficili da mantenere stabili durante la stampa. L’uso dell’alginato è coerente con molta letteratura sul drug delivery, perché si tratta di un materiale ampiamente studiato per biocompatibilità, capacità di incorporare farmaci e possibilità di essere impiegato in sistemi di rilascio locale e controllato anche in oncologia.
Che cosa mostra lo studio nei dati sperimentali
Secondo l’articolo scientifico, le formulazioni ottimizzate hanno prodotto particelle di circa 200–300 nanometri, con un’efficienza di incapsulamento moderata compresa tra 33% e 44%. Gli impianti stampati hanno mostrato un rilascio di doxorubicina più sostenuto rispetto alla sospensione del farmaco, mentre i test in vitro su cellule di carcinoma mammario MCF7 hanno evidenziato una riduzione della vitalità cellulare e una localizzazione intracellulare e nucleare coerente con il meccanismo d’azione della doxorubicina. In altre parole, il sistema non si limita a trattenere il farmaco: riesce a consegnarlo in un formato che, almeno in laboratorio, conserva attività citotossica contro le cellule tumorali.
Perché questo approccio interessa l’oncologia applicata
La logica di fondo è molto chiara: la chemioterapia sistemica resta efficace in molti contesti clinici, ma porta con sé una distribuzione nell’intero organismo che contribuisce agli effetti collaterali. La letteratura più ampia sugli idrogel impiantabili e iniettabili per terapia oncologica locale indica proprio questo come uno dei principali motivi di interesse: trasformare il materiale in un “depot” terapeutico, cioè in una riserva locale che mantenga il farmaco vicino alla lesione, con rilascio graduale e minore tossicità sistemica. In questo quadro, il lavoro della University of Mississippi si colloca come un tassello sperimentale che unisce biostampa, nanocarrier e rilascio controllato.
Che cosa manca prima di un possibile uso clinico
Il punto decisivo è che si tratta ancora di una ricerca in vitro. I ricercatori stessi spiegano che serviranno studi in vivo, verifiche sulla sicurezza, sulla degradazione del materiale, sulla dose realmente erogata nel tessuto tumorale e sulla riproducibilità della fabbricazione prima di ipotizzare un percorso clinico. Inoltre, il passaggio dalla prova di laboratorio a un impianto terapeutico impone requisiti severi su sterilità, standardizzazione produttiva e comportamento del dispositivo nell’organismo. Per questo il lavoro va letto come una prova di fattibilità avanzata, non come una tecnologia pronta all’uso ospedaliero.
Perché la notizia merita attenzione
L’aspetto più interessante non è solo la stampa 3D in sé, ma la combinazione tra manifattura additiva e formulazione farmaceutica. Qui la struttura stampata non è un semplice supporto meccanico: è parte attiva del sistema di somministrazione. Se questa impostazione troverà conferma in modelli animali e poi in studi clinici, potrebbe aprire spazio a impianti locali personalizzati per lesioni solide ben localizzate, in particolare nei casi in cui concentrare il farmaco in una sede precisa abbia vantaggi rispetto alla somministrazione sistemica. È una linea di ricerca che si inserisce in una tendenza più ampia della medicina di precisione: non solo scegliere il farmaco, ma controllare con maggiore precisione dove e come viene rilasciato.