Abstract
La stampa tridimensionale (3D) di impianti in titanio poroso sta aumentando in ortopedia, promettendo una migliore fissazione ossea mantenendo allo stesso modo somiglianze progettuali con componenti fabbricati in modo convenzionale. Il nostro studio è uno dei primi a caratterizzare in modo non distruttivo gli impianti stampati in 3D, utilizzando come riferimento componenti fabbricati in modo convenzionale.
metodi
Abbiamo analizzato 16 tazze acetabolari recuperate da pazienti, divise in due gruppi: “3D-stampato” ( n = 6) e “convenzionale” ( n = 10). La macchina di misurazione delle coordinate (CMM), la microscopia elettronica (SEM) e la tomografia microcomputer (micro-CT) sono state utilizzate per studiare la rotondità della superficie interna della coppa, la morfologia della superficie posteriore e le caratteristiche morfometriche delle strutture porose delle coppe , rispettivamente. È stata anche valutata la quantità di attaccamento osseo.
risultati
L’analisi CMM ha mostrato una rotondità mediana di 19,45 e 14,52 μm rispettivamente per bicchieri stampati in 3D e convenzionali ( p = 0,1114). Le immagini SEM hanno rivelato particelle parzialmente fuse sui montanti di impianti stampati in 3D; questi sono un sottoprodotto della tecnica di fabbricazione, a differenza delle perle mostrate dalle tazze convenzionali. Come previsto, la porosità, le dimensioni dei pori, lo spessore del montante e lo spessore della struttura porosa erano significativamente più alti per i componenti stampati in 3D ( p = 0,0002), con valori mediani del 72,3%, 915 μm, 498 μm e 1,287 mm ( p = 0,0002) . I valori mediani dell’attaccamento osseo erano rispettivamente dell’84,9% e del 69,3% per le coppe stampate in 3D e convenzionali ( p = 0,2635).
Conclusione
Gli impianti stampati in 3D sono progettati per essere significativamente più porosi di alcuni componenti convenzionali, come mostrato in questo studio, pur mostrando la stessa forma e dimensione. Abbiamo trovato differenze nelle morfologie superficiali dei gruppi, legate ai diversi metodi di fabbricazione; un risultato chiave è stata la presenza di particelle parzialmente fuse sulle coppe stampate in 3D.
sfondo
Oltre 100.000 componenti acetabolari e femorali in titanio sono stati impiantati in pazienti nel Regno Unito nel solo 2017 [ 1 ]. La maggior parte di questi impianti sono stati realizzati utilizzando metodi convenzionali come la lavorazione a controllo numerico computerizzato (CNC) di barre lavorate. Tuttavia, le tecnologie di produzione additiva (AM), note anche come stampa tridimensionale (3D), stanno rapidamente aumentando in ortopedia, in particolare nella produzione di componenti acetabolari porosi non cementati pronti all’uso per artroplastica totale dell’anca (THA) [ 2 , 3 , 4 , 5 ]. Secondo il National Joint Registry (NJR) del Regno Unito (UK) [ 1 , 6], circa l’11% e il 13% di tutte le coppe non cementate per le procedure di revisione eseguite nel 2017 e nel 2018, rispettivamente, sono state stampate in 3D.
La stampa 3D consente la fabbricazione di strutture e caratteristiche porose complesse che possono fornire una maggiore stabilità di fissazione, rispetto alle geometrie porose fabbricate convenzionalmente [ 3 ]. Le forme dei pori appositamente progettate possono essere prodotte utilizzando la stampa 3D, a differenza delle tecnologie tradizionali in cui vi è un controllo limitato sul layout della struttura porosa [ 7]. La logica clinica dietro l’uso della stampa 3D per impianti personalizzati (adattati al paziente) era quella di superare i limiti dei componenti personalizzati convenzionali, che non potevano affrontare casi complessi in cui il materiale osseo era molto limitato. Considerando le tazze standard, la principale logica clinica è quella di creare strutture porose che massimizzino l’integrazione ossea, specialmente nelle procedure di revisione. Inoltre, la stampa 3D consente il massimo controllo sul design della coppa, come fori con bordi rinforzati e pareti della coppa più sottili per un dato diametro della coppa, consentendo ai chirurghi di usare teste femorali più grandi [ 8 ]
Dal punto di vista ingegneristico, la stampa 3D limita l’uso di strumenti specializzati e complesse procedure di assemblaggio, considerando che le strutture dense e porose sono costruite in un unico passaggio. Ciò riduce il costo del componente finale, senza influire sulla maggiore complessità della struttura. Se con questa tecnologia è possibile ottenere una semplificazione della produzione più economica, in particolare quando viene prodotto un piccolo numero di parti, tuttavia, la post-elaborazione successiva alla produzione principale rappresenta ancora un onere per il costo finale [ 2 , 7 , 8 , 9 , 10 ].
La stampa 3D consente la progettazione e la produzione di strutture complesse e dimensioni ottimizzate delle tazze, ma i suoi rischi potenziali e l’impatto clinico sono ancora poco conosciuti [ 11 ].
Recenti studi clinici su tazze stampate in 3D hanno mostrato buoni risultati [ 12 , 13 , 14 , 15 ]; tuttavia, nessuno studio di laboratorio ha precedentemente caratterizzato tutti i componenti. Al contrario, diversi studi hanno studiato la biocompatibilità e l’idoneità della stampa 3D per produrre strutture porose per applicazioni ortopediche, ma queste erano limitate a campioni cilindrici o cubici [ 7 , 16 , 17 , 18 , 19 , 20 , 21 , 22 , 23 , 24 , 25 , 26 ],
Lo scopo di questo studio era di comprendere meglio le proprietà delle coppe ortopediche stampate in 3D, caratterizzandone il design e fornendo risultati preliminari che potrebbero rappresentare la loro interazione con l’osso. Utilizzando come riferimento una serie di tazze prodotte in modo convenzionale, abbiamo valutato (1) una caratteristica dimensionale della superficie interna della tazza, che potrebbe influire sulla sede del rivestimento; (2) morfologia superficiale e struttura porosa sul retro delle coppe, che sono correlate all’osteointegrazione; (3) la quantità di attaccamento osseo, come primo indicatore dell’interazione osso-impianto.
Materiali e metodi
Il disegno dello studio è presentato in Fig. 1 . È stata ottenuta l’approvazione da parte del comitato di revisione istituzionale del protocollo umano per questa indagine (London-Riverside REC 07 / Q0401 / 25).
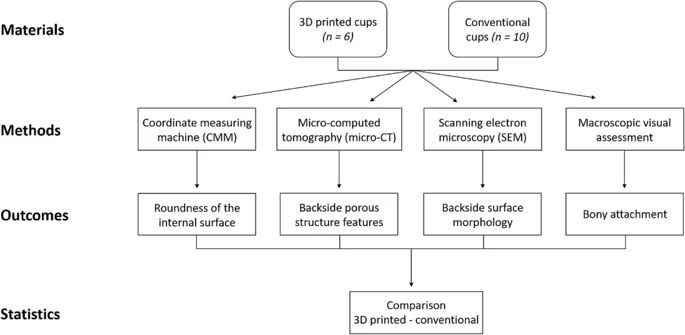
materiale
Questo studio ha esaminato 16 tazze acetabolari di titanio-alluminio-vanadio (Ti6Al4V) ricevute presso il nostro centro dopo essere state recuperate dai pazienti. Sebbene questa non sia stata un’indagine di recupero, la raccolta di impianti recuperati ci ha permesso di analizzare i progetti di diversi produttori. Le coppe sono state divise in due gruppi in base al loro metodo di produzione: “3D-stampato” ( n = 6; Delta TT; Lima Corporate, Udine, Italia) e “convenzionale” ( n = 10; Pinnacle Porocoat; DePuy Synthes, Raynham, STATI UNITI D’AMERICA). Gli impianti stampati in 3D avevano una dimensione mediana (intervallo interquartile — IQR) di 54 mm (da 50 a 56,5) e sono stati prodotti utilizzando la fusione a fascio di elettroni (EBM) [ 16 ]. Questo disegno acetabolare stampato in 3D è il più utilizzato nel Regno Unito secondo NJR [ 1]. Le coppe convenzionali avevano una dimensione mediana (IQR) di 54 mm (da 52 a 56,5) e venivano fabbricate forgiando e lavorando il guscio acetabolare e sinterizzando il rivestimento posteriore [ 27 ]; questo design convenzionale non cementato è uno dei più utilizzati nel Regno Unito [ 1 ].
I pazienti nei gruppi stampati in 3D e convenzionali avevano un’età mediana (IQR) di 61,1 (48,3-71,6) e 67,2 (63,3-70,1) anni ( p = 0,5941), un tempo mediano (IQR) per la revisione di 24,9 (21,1- 46,8 ) e 49 (da 23,8 a 62,1) mesi ( p = 0,296) e i sessi erano rispettivamente del 20% e del 43% maschi. Le ragioni della revisione includevano dolore inspiegabile, allentamento asettico e infezione per il gruppo stampato in 3D; reazione avversa a detriti metallici (ARMD), allentamento asettico e dolore inspiegabile per quello convenzionale.
Rotondità della superficie interna della tazza
Una macchina di misurazione delle coordinate (CMM) Zeiss Contura (Carl Zeiss Ltd, Rugby, Regno Unito) è stata utilizzata per misurare la rotondità della superficie interna della tazza. Le misurazioni sono state eseguite utilizzando uno stilo rubino da 2 mm, registrando 3 tracce a diverse altezze dal bordo per ciascun componente, con una media di 14.756 punti per ogni traccia. L’accuratezza della tecnica di misurazione era 2,2 + L / 350 μm, dove L è la dimensione misurata. I valori di rotondità sono stati calcolati automaticamente utilizzando il metodo del cerchio di zona minimo (differenza tra il raggio dei punti più interni ed esterni del profilo).
Morfologia della superficie posteriore
Una microscopia elettronica a scansione: SEM (Hitachi S3400-N, Tokyo, Giappone) è stata utilizzata per un’analisi dettagliata della morfologia superficiale degli impianti. Le immagini sono state catturate in modalità SEI (Electronic Electron Imaging) a 20 kV, con ingrandimenti che vanno da × 30 a × 180.
Struttura porosa sul retro della tazza
L’analisi della tomografia micro-computata (micro-CT) è stata utilizzata per studiare le caratteristiche morfometriche delle strutture porose sul retro degli impianti. Il metodo prevedeva tre fasi: (1) scansione micro-CT dei componenti acetabolari e ricostruzione dei dati, (2) segmentazione e rendering volumetrico dei dati micro-CT e (3) misurazione dei parametri morfometrici delle strutture porose.
Scansione Micro-CT
Gli impianti sono stati scansionati utilizzando uno scanner micro-CT (XTH 225, Nikon Metrology NV) impostato a 150 kV, con una corrente del fascio di 70 μA. Le scansioni includevano 3177 viste con incrementi di 0,11 °, con un fotogramma per vista ed esposizione di 1000 ms. La scansione di oggetti metallici è influenzata da un effetto di indurimento del raggio, che comporta l’attenuazione dei fotoni a bassa energia (cioè i raggi X morbidi) mentre il raggio dei raggi X si muove attraverso il materiale assorbente [ 28 ]. Al fine di ridurre questo effetto , è stato utilizzato un filtro Cu fisico di 0,25 mm, situato alla sorgente del fascio; un algoritmo (correzione polinomiale del quarto ordine) è stato applicato anche durante il processo di ricostruzione. La ricostruzione delle scansioni è stata eseguita a una risoluzione isotropica completa di 35 μm.
La scelta dei parametri di scansione micro-CT per i campioni di titanio manca di conformità generale [ 28 ]; pertanto, uno degli impianti è stato scansionato tre volte utilizzando diversi set di tensione e corrente: 80 kV, 200 μA; 100 kV, V100 μA; 150 kV, 70 μA. I valori sono stati scelti in base alla letteratura [ 29 ], coprendo la gamma consentita dallo scanner ed evitando la saturazione delle immagini. I risultati sono stati confrontati semiquantitativamente, in termini di (1) presenza del picco corrispondente all’oggetto metallico nel diagramma dell’istogramma del conteggio del voxel rispetto all’intensità del voxel (livello di grigio) e (2) aspetto dei volumi renderizzati.
Il diagramma dell’istogramma mostrava un picco più elevato corrispondente al campione di metallo quando si utilizzava l’insieme di parametri 150 kV, 70 μA (Fig. 2 ), implicando una migliore separazione tra voxel appartenenti allo sfondo (aria) e voxel relativi al campione di titanio. I volumi renderizzati hanno confermato il risultato precedente, con tutte le caratteristiche dell’impianto chiaramente visibili senza alcun rumore. Il set 150 kV, 70 μA è stato quindi scelto per la scansione di tutti gli impianti.
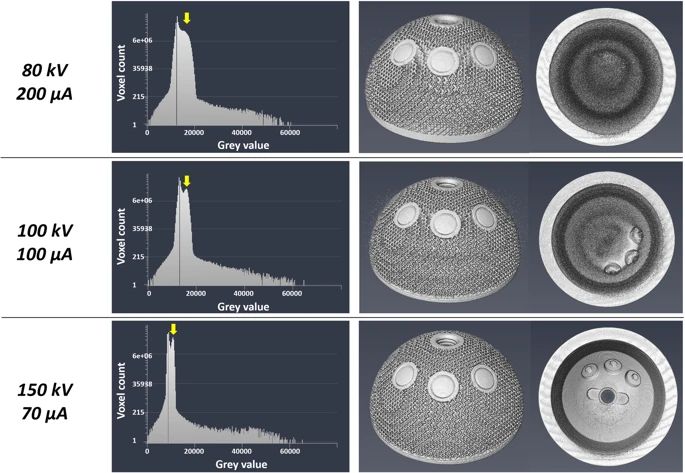
Immagini che mostrano i risultati del processo di ottimizzazione dei parametri di scansione micro-CT. Dall’alto verso il basso, i parametri studiati erano 80 kV, 200 μA, 100 kV, 100 μA e 150 kV, 70 μA. È stato scelto l’insieme di valori 150 kV, 70 μA perché il picco corrispondente al metallo (freccia gialla) nell’istogramma del conteggio del voxel era più alto rispetto allo stesso picco nei grafici relativi all’altra serie di parametri. Un picco più elevato suggeriva una migliore separazione tra voxel appartenenti allo sfondo (aria) e voxel appartenenti al materiale. Il volume ricostruito ottenuto con i valori di 150 kV, 70 μA ha fornito una rappresentazione più chiara dell’impianto rispetto agli altri
Segmentazione e rendering del volume
Le scansioni ricostruite degli impianti sono state segmentate e rese utilizzando un software di analisi micro-CT 3D (Avizo 9.0, Thermofisher Scientific, USA). La segmentazione è stata eseguita scegliendo un valore di bordo grigio specifico per ciascun impianto, utilizzando un processo di segmentazione automatico basato sul principio “iso-50” [ 28 ]. Il valore di soglia corrispondeva al livello medio-grigio tra i picchi che coincidono con i materiali irradiati (nel nostro caso lega di titanio e aria come sfondo) nel diagramma dell’istogramma dei conteggi dei voxel rispetto all’intensità del voxel.
Misura dei parametri morfometrici della struttura porosa
I modelli ricostruiti in 3D sono stati usati per valutare le caratteristiche morfometriche clinicamente rilevanti della struttura porosa degli impianti: (1) porosità , che è la percentuale di spazio vuoto in un volume, (2) dimensione dei pori , calcolata come il diametro dei pori e (3) spessore del puntone , che è la dimensione delle singole parti che compongono la struttura porosa (nelle coppe convenzionali, queste caratteristiche sono state misurate considerando i montanti approssimativi creati dalle perle imballate che formano il rivestimento posteriore). La porosità e la dimensione dei pori rappresentano lo spazio disponibile per la crescita ossea; lo spessore del puntone è il sito per l’attacco delle cellule ossee. Lo spessore della struttura porosa è stato anche misurato, che rappresenta la massima profondità di penetrazione per il tessuto osseo.
Le misurazioni sono state eseguite utilizzando un software di analisi micro-CT 3D (Avizo 9.0, Thermofisher Scientific, USA) e un software di dominio pubblico per l’analisi delle immagini (ImageJ 1.52a, Broken Symmetry Software) selezionando il volume di interesse limitando solo la rete porosa e sezioni degli impianti. Complessivamente, sono state eseguite 85 misurazioni su ciascun componente.
Analisi macroscopiche: valutazione visiva della crescita dei tessuti
L’area di attacco del tessuto osseo è stata misurata utilizzando un metodo fotogrammetrico che include un sistema di imaging (fotocamera EOS 5D Mark II, Canon, Tokyo, Giappone) e un software di dominio pubblico per l’analisi delle immagini (ImageJ 1.52a, Broken Symmetry Software). La calibrazione dell’immagine è stata eseguita posizionando una scala di riferimento nel campo visivo. Una percentuale complessiva di attaccamento osseo è stata calcolata facendo la media delle misurazioni da quattro aree in cui le coppe sono state divise in; la presenza di osso era marcata solo quando era visibile una struttura porosa bianca (cioè chiara evidenza di tessuto osseo).
analisi statistica
L’analisi statistica è stata eseguita usando Prism 7 (GraphPad, USA). Le differenze tra coppe stampate in 3D e convenzionali in termini di rotondità della superficie interna della coppa, caratteristiche morfometriche delle strutture porose (porosità, dimensione dei pori, spessore del montante), spessore della struttura porosa e attacco del tessuto osseo sono state valutate usando non parametrici Test di Mann-Whitney. Il livello di significatività per tutte le analisi statistiche era p <0,05. Va notato che la piccola dimensione del campione in entrambi i gruppi potrebbe influenzare i risultati statistici, non consentendo di trarre conclusioni definitive. Pertanto, i risultati dell’analisi statistica dovrebbero essere considerati solo un’indicazione descrittiva del confronto tra coppe stampate in 3D e convenzionali.
risultati
La sezione “Risultati” viene presentata in base alla posizione studiata sui componenti acetabolari, a partire dall’analisi eseguita sulla superficie interna della coppa e proseguendo con l’indagine della parte posteriore delle coppe stampate in 3D e convenzionali.
Rotondità della superficie interna della tazza
Dall’analisi della superficie interna della coppa mediante CMM, sono state ottenute rotondità mediana (IQR) di 19,45 μm (da 15,69 a 37,30) e 14,52 μm (da 12,59 a 16,79) rispettivamente per impianti stampati in 3D e convenzionali ( p = 0,1114) .
Morfologia della superficie posteriore
Come previsto, l’analisi SEM ha rivelato differenze nella morfologia superficiale tra coppe stampate in 3D e convenzionali; le immagini catturate sono mostrate in Fig. 3 .
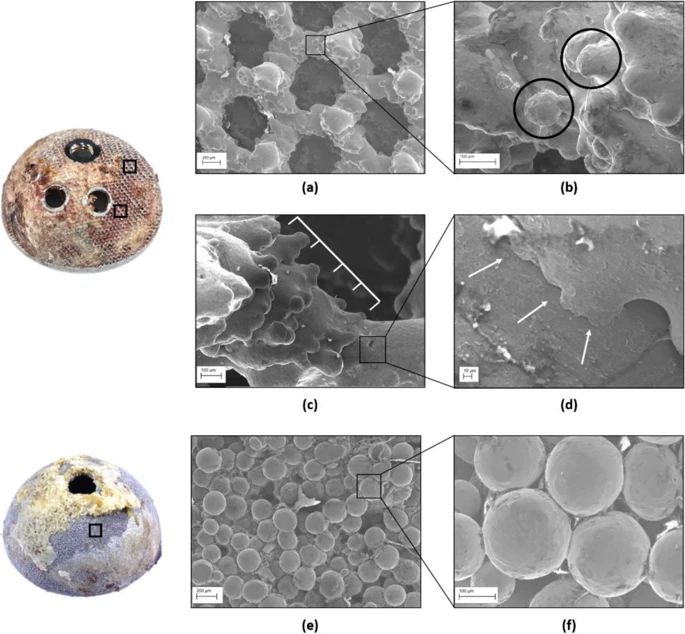
Immagini SEM di un impianto stampato in 3D e di un impianto convenzionale. a La struttura porosa stampata in 3D aveva una forma regolare con pori chiaramente identificabili; b particelle parzialmente fuse (cerchi neri) erano visibili sui montanti; c l’effetto ‘gradino’ dovuto alla produzione strato su strato e ( d ) le linee di trama sono state trovate anche con ingrandimento maggiore. Diversamente, tazze convenzionali mostravano e meno chiaramente identificabili pori e f perline di distribuzione uniforme lungo tutta la superficie posteriore
Immagine a dimensione intera
A basso ingrandimento, la superficie posteriore delle coppe nel gruppo stampato in 3D mostrava una struttura porosa regolare, con un motivo ripetuto di pori che assomigliano approssimativamente a celle unitarie a forma esagonale. Gli impianti nel gruppo convenzionale hanno mostrato una morfologia diversa, con pori meno visibili tra le perle impaccate che formano la parte posteriore.
A un ingrandimento più elevato, tutte le coppe acetabolari stampate in 3D mostravano particelle di posizione non uniforme attaccate ai puntoni della struttura porosa; la dimensione mediana (IQR) di queste particelle era di 73 μm (da 68 a 89).
Sulle coppe convenzionali erano presenti anche perline, ma distribuite uniformemente sulla superficie posteriore e di dimensioni mediane maggiori (IQR), pari a 208 μm (da 196 a 225).
L’effetto ‘gradino’ dovuto al processo di fabbricazione strato su strato e le linee di trama tra strati consecutivi sono stati osservati anche sulla superficie dei montanti che compongono la struttura porosa delle coppe stampate in 3D; queste caratteristiche non erano presenti sulla superficie degli impianti fabbricati in modo convenzionale.
Struttura porosa sul retro della tazza
L’analisi micro-CT ha confermato che i componenti acetabolari appartenenti ai due gruppi avevano strutture porose molto diverse, come osservato dalle immagini SEM. Le coppe stampate in 3D mostravano una struttura regolare con pori riconoscibili, mentre gli impianti convenzionali presentavano una superficie posteriore irregolare, con perline circolari identificabili e pori meno visibili (Fig. 4 ).
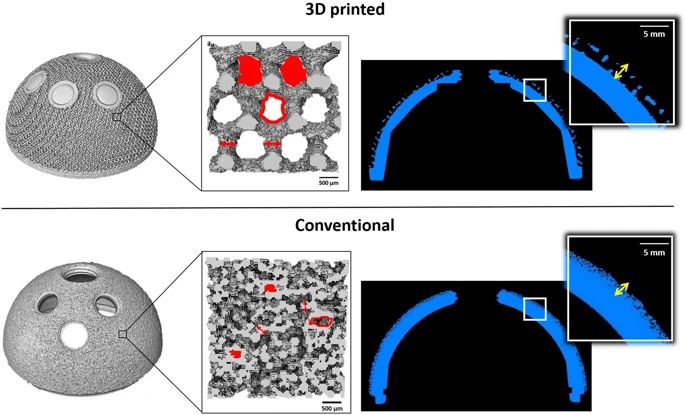
Immagini che mostrano i risultati dell’analisi micro-CT delle coppe stampate in 3D (sopra la linea continua) e convenzionali (sotto la linea continua). Da sinistra a destra, sono esposti tutti gli impianti ricostruiti e uno zoom sulle strutture porose con i parametri morfometrici rappresentati (porosità, dimensione dei pori, spessore del montante). La porosità è definita come la percentuale del volume vuoto (forme riempite di rosso) rispetto al volume totale; la dimensione dei pori è il diametro del cerchio la cui area è uguale a quella delle forme vuote rosse; e lo spessore del puntone è indicato dalle frecce rosse. Sono anche mostrati una sezione trasversale dei componenti e uno zoom che mostra lo spessore della struttura porosa (frecce gialle). Le coppe stampate in 3D hanno mostrato strutture porose più porose e più spesse
Immagine a dimensione intera
Le misurazioni mediane delle caratteristiche morfometriche valutate per le strutture porose sul retro dei due gruppi di tazze sono riassunte nella Tabella 1 .
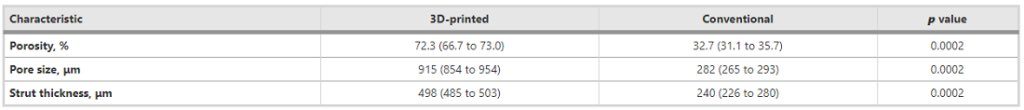
Tabella 1 Misure mediane (IQR) delle caratteristiche morfometriche delle strutture porose di impianti stampati in 3D e convenzionali
Tavolo a grandezza naturale
La porosità delle tazze stampate in 3D era il doppio del valore mostrato dalle tazze convenzionali e queste differenze erano statisticamente significative ( p = 0,0002). Allo stesso modo, lo spessore dei montanti che compongono la struttura porosa delle coppe convenzionali era metà della dimensione mostrata dagli impianti stampati in 3D, con una differenza significativa tra i due gruppi ( p <0,0002). Inoltre, i componenti convenzionali avevano pori di tre volte più piccoli di diametro rispetto alle coppe stampate in 3D ( p = 0,0002).
I componenti stampati in 3D hanno anche mostrato una struttura porosa più spessa, con un valore mediano (IQR) di 1.287 mm (da 1.263 a 1.291) rispetto a 0.940 mm (da 0.897 a 0.964) delle coppe convenzionali. Questa differenza era significativa ( p = 0,0002). La distribuzione dello spessore della struttura porosa misurata per entrambi i gruppi è presentata in Fig. 5 .
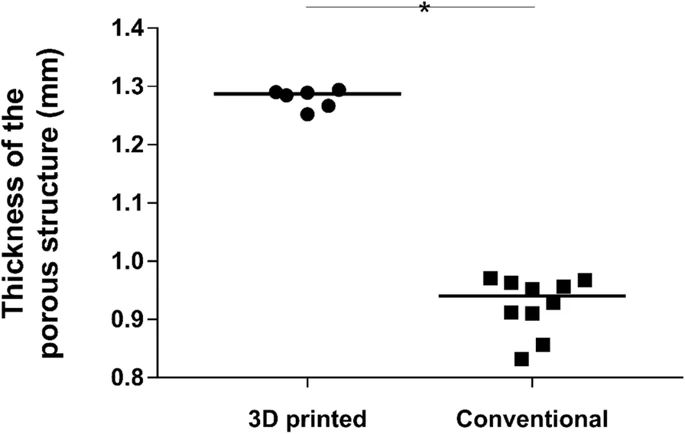
Dot plot che mostra la distribuzione dei valori di spessore della struttura porosa misurata per i due gruppi. La linea continua rappresenta il valore mediano. Gli impianti stampati in 3D hanno mostrato una struttura significativamente più spessa rispetto alle coppe convenzionali ( p = 0,0002)
Immagine a dimensione intera
Dalle sezioni micro-CT sono state identificate anche aree con valori di scala dei grigi diversi dal materiale dell’impianto (Ti6Al4V) e dall’aria di fondo (Fig. 6 ).
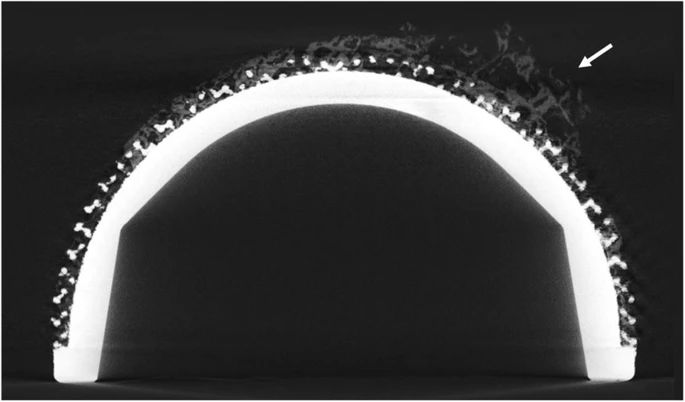
Immagine che mostra una sezione CT di una tazza stampata in 3D con aree grigie (frecce bianche) raffigurante la presenza di un materiale diverso dalla lega Ti6Al4V e dall’aria di fondo
Immagine a dimensione intera
Confronto usando il test di Mann-Whitney
Valutazione visiva macroscopica dell’attaccamento osseo
Le coppe stampate in 3D e convenzionali presentavano una copertura mediana (IQR) della superficie ossea di attacco dell’84,9% (da 65 a 95,6) e del 69,3% (da 65,1 a 93,9), rispettivamente ( p = 0,2635). Esempi di percentuali alte e basse di attaccamento osseo sono rappresentate in Fig. 7 .
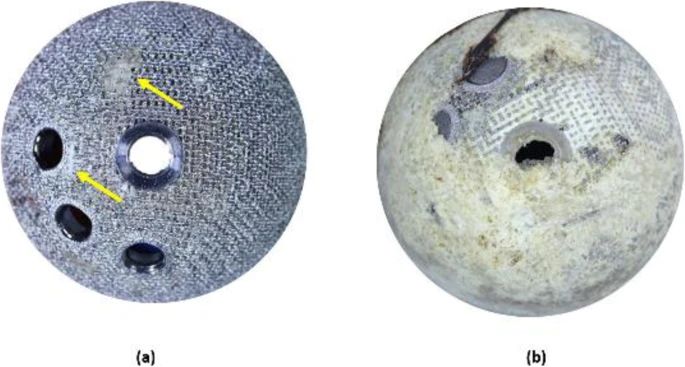
Immagine che mostra un esempio di un basso e b un’alta percentuale di inserzione ossea sulle tazze 3D-stampate. La presenza di osso nell’immagine a è indicata dalle frecce gialle
Immagine a dimensione intera
I dati relativi a ciascuna coppa (sesso, età del paziente, tempo di revisione, parametri morfometrici, spessore della struttura porosa e attacco osseo) sono riportati nella Tabella 2 della sezione Appendice.
Discussione
Questo è uno dei primi studi a caratterizzare i componenti acetabolari ortopedici stampati in 3D per il THA; componenti comunemente usati di fabbricazione convenzionale sono stati usati come riferimento per evidenziare le caratteristiche di questi nuovi tipi di impianti. Le coppe fabbricate in modo convenzionale con superfici posteriori porose sono state clinicamente adottate per circa 40 anni [ 30 ], mostrando buoni risultati complessivi [ 31 ], essendo quindi un valido punto di riferimento per valutare le proprietà degli impianti stampati in 3D che potrebbero influenzarne i risultati clinici. Sebbene l’adozione clinica delle coppe stampate in 3D non sia ancora diffusa, diversi modelli acetabolari stampati in 3D sono ora disponibili sul mercato e il loro uso dovrebbe crescere rapidamente.
In questo studio, l’uso di tazze recuperate ci ha permesso di indagare su progetti che sarebbero altrimenti scarsamente disponibili, in particolare gli impianti stampati in 3D. Un metodo di analisi non distruttivo che coinvolge imaging CMM, SEM e micro-CT è stato utilizzato per studiare le proprietà relative alla sede del rivestimento interno e caratteristiche che influenzano l’osteointegrazione e la stabilità dell’impianto.
Come previsto, abbiamo trovato differenze nelle proprietà morfometriche delle strutture porose, con il doppio della porosità, il triplo della dimensione dei pori e il doppio dello spessore del puntone nelle coppe stampate in 3D. La struttura porosa era anche più spessa rispetto alle coppe convenzionali. Sebbene queste caratteristiche morfometriche facciano parte dell’attuale protocollo di stampa 3D, rimangono delle domande su cosa sia ottimale per l’integrazione osso-protesi. È interessante notare che abbiamo identificato particelle parzialmente attaccate ai montanti dei componenti stampati in 3D; questo è un risultato non voluto del processo stampato in 3D. L’analisi visiva preliminare dell’attaccamento osseo ha rivelato una percentuale simile per i due gruppi di impianti.
La rotondità comparabile della superficie interna delle coppe stampate in 3D e convenzionali ha suggerito che i diversi metodi di produzione non hanno influenzato questa proprietà dimensionale. È stata tuttavia misurata una gamma più ampia di valori per i bicchieri stampati in 3D; non è chiaro se ciò rappresenti una vera differenza tra i due gruppi, dato il basso numero di impianti inclusi in questo studio. Complessivamente, la superficie interna delle coppe sia stampate in 3D che convenzionali è lavorata per ottenere le tolleranze specifiche prescritte dal produttore [ 27]. Inoltre, una rotondità comparabile tra i due gruppi ha suggerito che le coppe non si deformavano in situ. Il guscio può deformarsi al momento dell’inserimento in determinate condizioni e un’errata sede del rivestimento può causare la sua frattura (se ceramico) o influire negativamente sulla lubrificazione del film fluido, con conseguente aumento dell’usura [ 32 ]. Abbiamo trovato valori mediani inferiori a 20 μm per entrambi i gruppi; sebbene le tolleranze dimensionali per questa funzione non fossero disponibili, tuttavia potremmo concludere che tutte le tazze presentavano una superficie interna rotonda quasi perfetta.
In termini di proprietà morfologiche, entrambi i gruppi hanno mostrato la presenza di particelle. La differenza fondamentale è che le perle presenti sugli impianti convenzionali sono destinate a formare la struttura porosa (Porocoat) sul retro delle coppe: le perle di titanio sono state sinterizzate sul substrato Ti6Al4V (parte densa del guscio) in un costrutto multistrato via alto – cicli di temperatura in un forno a vuoto. Il processo ha indotto la diffusione allo stato solido con il substrato e tra i granuli [ 33]. Al contrario, le particelle parzialmente fuse sulle tazze stampate in 3D sono un sottoprodotto del processo di fabbricazione: alcune delle particelle di polvere che compongono la materia prima di partenza del processo di stampa 3D non sono state completamente fuse insieme. Queste particelle, insieme alle linee di trama, erano state precedentemente osservate in campioni fabbricati con EBM [ 34 , 35 , 36 ]. Le linee di trama sono state create dalla fabbricazione strato per strato (“effetto gradino”) e dal piccolo movimento della vasca di fusione durante il processo di costruzione. La fonte di energia (in questo caso raggio di elettroni) ha fuso la polvere metallica, seguendo il percorso fornito dal file CAD (computer-aided design) e ha creato aree di materiali fusi (pool) che sono soggetti a piccoli movimenti [ 36 ].
In generale, queste caratteristiche morfologiche forniscono una superficie ruvida che può favorire l’adesione e la crescita delle cellule di osteoblasti (osteoconduzione), come precedentemente dimostrato per questo specifico materiale specifico [ 23 , 24 ]. Ciò rientra nel principio materiale della “guida di contatto”, in base al quale il movimento e lo sviluppo delle cellule sono influenzati dalla morfologia superficiale dell’impianto [ 37 ]. Tuttavia, un recente studio in vitro di Xie et al. [ 38] ha suggerito che la presenza di particelle parzialmente fuse non solo ha migliorato l’adesione batterica, ma ha anche inibito l’attività osteogena delle cellule staminali mesenchimali ossee umane, raccomandando così di rimuovere le particelle. Anche il potenziale rilascio di queste particelle non può essere escluso, come suggerito da Matouskova et al. [ 18 ]; ciò può comportare un aumentato rischio di reazioni infiammatorie o una ridotta emocompatibilità [ 18] o a livelli di metallo (titanio) elevati nel sangue. L’elevata superficie del metallo esposto data dall’elevata porosità della struttura trabecolare dei componenti stampati in 3D può aumentare questo processo di rilascio. Ad oggi, l’unico studio che ha studiato la possibilità di aumentare il livello di metallo sistemico (titanio) in pazienti con coppe Delta TT a causa dell’architettura altamente porosa non ha trovato risultati significativi [ 39 ].
Per quanto a conoscenza degli autori, il problema delle particelle parzialmente fuse non è stato ancora affrontato da nessuno degli organismi di regolamentazione, come la Food and Drug Administration (FDA) negli Stati Uniti, l’Agenzia europea per i medicinali (EMA) nell’Unione europea o la Medicine and Healthcare Products Regulatory Agency (MHRA) nel Regno Unito, né da organizzazioni di standardizzazione, come la American Society for Testing and Material (ASTM), la International Organization for Standardization (ISO) o la British Standards Institution (BSI). La FDA ha pubblicato le linee guida generali sui dispositivi medici fabbricati con additivi alla fine del 2017 [ 40 ] e sono stati pubblicati standard su terminologia, progettazione, processo, materiali e metodi di prova per parti stampate in 3D [ 8]. Tuttavia, manca ancora un regolamento approfondito.
Come previsto, sono state trovate differenze tra coppe stampate in 3D e coppe convenzionali per tutti i parametri morfometrici e lo spessore della struttura porosa. Il rivestimento Porocoat rappresenta una soluzione tradizionale per ottenere un retro poroso su una coppa acetabolare non cementata, con perle di titanio sinterizzate su una calotta Ti6Al4V. Le proprietà morfometriche di questo rivestimento, come definito dal produttore, comprendono una dimensione media dei pori di 250 μm, una porosità media del volume del 45% e una profondità del rivestimento di 0,762 ± 0,254 mm ( media ± sd ) [ 27 ]; questi sono paragonabili ai valori misurati nel nostro studio. L’influenza della porosità e della dimensione dei pori sulla crescita ossea e sull’osteointegrazione dell’impianto è un argomento controverso [ 41], ma i valori morfometrici mostrati dal rivestimento Porocoat rientrano nell’intervallo 100–400 μm che è stato suggerito da studi in vitro e in vivo per avere la dimensione ottimale dei pori [ 42 , 43 , 44 ]. In effetti, il componente acetabolare Pinnacle Porocoat è stato ampiamente utilizzato nelle procedure primarie dell’anca eseguite nel Regno Unito nel 2017 (28% di tutte le coppe non cementate) [ 1 ], e questo rivestimento è stato applicato a diversi modelli di coppe acetabolari da oltre 30 anni [ 27 , 45 ], con buoni risultati clinici [ 46 ].
La coppa acetabolare Delta TT ha una parte posteriore molto porosa che mira a raggiungere la fissazione in interventi sia primari che di revisione. La struttura reticolare di queste coppe è una matrice regolare composta da esagoni multi-planari chiamati Trabecular Titanium (TT), che in precedenza erano stati caratterizzati utilizzando campioni cilindrici e cubici. Marin et al. [ 16] ha preso in considerazione due strutture TT (“piccola” e “grande”) al fine di studiare l’idoneità del processo AM a produrre una struttura porosa per applicazioni ortopediche. Hanno riportato porosità del 63,2 ± 1,3% e 72 ± 0,8% e dimensioni dei pori di 0,64 ± 0,11 mm e 1,43 ± 0,07 mm per il primo e il secondo, rispettivamente. Questi valori sono paragonabili alla porosità e alle dimensioni dei pori misurate nel nostro studio. Le nostre misure di spessore del montante sono state trovate simili a un altro studio di Regis et al. [ 26 ] che ha riportato un valore di 355 ± 10 μm. I valori suggeriti della capacità di tolleranza della tecnologia EBM (± 250/300 μm) supportano queste affermazioni [ 16 , 26 ].
Gli studi clinici di follow-up relativi al design acetabolare Delta TT hanno mostrato buoni esiti precoci e intermedi. Steno et al. [ 12 ] hanno riferito dei primi risultati (periodo di follow-up medio di 38,14 mesi) di 81 casi di revisione in cui è stata eseguita una sola revisione a causa dell’instabilità del componente acetabolare. Perticarini et al. [ 13 ] hanno riscontrato che il 99,3% delle coppe Delta TT utilizzate in 134 casi di THA e 8 casi di revisione erano radiograficamente stabili ad un periodo medio di follow-up di 72,7 mesi; lussazione avvenuta in due casi, allentamento asettico in un paziente. Munegato et al. [ 15 ] hanno descritto buoni risultati clinici e radiografici al follow-up a breve e medio termine (periodo medio 39,8 mesi), con tre casi di lussazione.
In generale, lo scopo di tutti i design acetabolari non cementati è quello di garantire (1) una buona stabilità primaria, che dipende dal raccordo tra la coppa e l’osso ospite e dal coefficiente di attrito della superficie posteriore con l’osso [ 45 ] e (2 ) fissazione a lungo termine con osso. Ciò è fortemente influenzato dalle caratteristiche morfometriche della struttura porosa come la porosità e la dimensione dei pori. L’osso trabecolare umano è costituito da uno spazio tridimensionale, interconnesso e aperto-poroso, con elevata porosità (50–90%), grandi dimensioni dei pori (nell’ordine di 1 mm) e spessore trabecolare (puntone) di centinaia di micron [ 47 , 48]. Il gruppo stampato in 3D ha mostrato valori morfometrici simili a quelli dell’osso trabecolare. È interessante notare che abbiamo identificato un terzo materiale, diverso da Ti6Al4V e l’aria di fondo, nelle sezioni trasversali delle coppe stampate in 3D ottenute dall’indagine micro-CT. Questi risultati preliminari suggeriscono che questo potrebbe essere l’osso che è cresciuto nella struttura porosa delle coppe, perché solo un materiale abbastanza denso da attenuare i raggi X in arrivo sarebbe visibile nelle fette CT. Ulteriori indagini forniranno uno spaccato di queste osservazioni.
Porosità, dimensione dei pori e interconnettività dei pori sono caratteristiche chiave che influenzano l’interazione tra l’impianto e il tessuto osseo. Questi parametri sono direttamente collegati alle proprietà meccaniche e alle prestazioni biologiche dell’impianto, influenzando il reclutamento, l’adesione e la proliferazione delle cellule ossee ( osteogenesi da contatto ), nonché il potenziale di vascolarizzazione e perfusione [ 41 , 49 ]. La logica per avere una struttura porosa su impianti ortopedici è quella di aumentare la fissazione e la stabilità a causa dell’interblocco meccanico creato dall’osso che cresce nella struttura [ 37]. La dimensione dei pori determina quali cellule colonizzeranno il materiale, influenzando direttamente la progressione del processo osteogenico. È stato riferito che i pori di 10–75 μm promuovono la crescita del tessuto fibroso; il tessuto osseo non mineralizzato penetra nei pori di 75–100 μm; e l’osso mineralizzato inizia a formarsi in pori di ~ 100 μm, con un’infiltrazione ossea ottimale nell’intervallo 100–500 μm [ 42 , 43 , 44 , 50 , 51 ]. Un recente studio sugli animali di Tanzer et al. [ 25 ] hanno descritto una crescita ossea consistente (> 50%) in una struttura porosa stampata in 3D con porosità dal 50 al 65% e dimensioni medie dei pori di 450 μm. Pertanto, è accettato che la formazione di osso lamellare richiede una dimensione dei pori di almeno alcune centinaia di micron [49 , 52 ]. Tuttavia, altri studi hanno suggerito che le dimensioni dei pori nell’intervallo 500-900 μm facilitano la crescita ossea e possono portare a una maggiore infiltrazione o una migliore risposta cellulare rispetto alla struttura con pori più piccoli [ 17 , 19 , 21 ]. È stato anche dimostrato che la formazione di tessuto fibroso si verifica con pori più grandi di 1000 μm [ 43 , 48 ] e un limite superiore in termini di dimensione dei pori dovrebbe essere impostato anche in relazione alle proprietà meccaniche. Questo è il motivo per cui la dimensione ottimale dei pori per la crescita ossea è ancora un argomento controverso in letteratura [ 41]. Complessivamente, la porosità e la dimensione dei pori ottimali da sole non comportano un’osteointegrazione dell’impianto di successo ma costituiscono due dei parametri principali nella categoria dei fattori “impianto”. Altri fattori correlati al “chirurgo” e al “paziente” influenzano ugualmente l’esito clinico finale, come la tecnica chirurgica (ad esempio approccio anteriore o posteriore), la scelta dell’impianto e la pianificazione dell’operazione o l’età del paziente, le condizioni cliniche, la qualità delle ossa e l’afflusso di sangue [ 49 ].
Uno dei principali vantaggi della tecnologia di stampa 3D è la possibilità di progettare e produrre in modo controllato una struttura porosa che assomiglia alle proprietà dell’osso, come riportato da numerosi studi [ 2 , 7 , 16 , 20 , 26 , 34 , 35 , 41 ]. Possono essere fabbricate sia strutture regolari (celle unitarie ripetute) sia irregolari (stocastiche); l’ottimizzazione della topologia, in cui un modello matematico fornisce le proprietà desiderate pur soddisfacendo i vincoli prescritti, può essere utilizzata anche [ 8 , 41 ].
Tuttavia, la libertà di progettazione potenzialmente illimitata garantita dalla stampa 3D non implica che la qualità della struttura porosa finale sia adatta per applicazioni mediche e ciò dipende dal design stesso e dai parametri di fabbricazione.
Nonostante le differenze (ovvero maggiore porosità, dimensione dei pori e spessore della struttura porosa per le coppe stampate in 3D), i disegni acetabolari hanno mostrato un attacco osseo comparabile, suggerendo un comportamento simile con l’osso in situ. È da notare che le coppe stampate in 3D hanno mostrato un valore mediano più elevato (85% vs 69%) nonostante il tempo mediano inferiore per la revisione (24 vs 49 mesi), sebbene questa differenza non fosse significativa. Ulteriori studi, inclusi più componenti acetabolari, fornirebbero migliori approfondimenti sull’argomento.
La tecnica chirurgica applicata per rimuovere le coppe non è stata considerata in grado di influenzare questo risultato, poiché è stata presa in considerazione anche la valutazione del tessuto all’interno delle strutture porose a livello della superficie. In uno studio comparativo retrospettivo, Swarts et al. [ 53 ] ha studiato visivamente la quantità di crescita dei tessuti su disegni acetabolari convenzionali recuperati, trovando una forte associazione tra il tipo di superficie porosa del guscio e la quantità di tessuto. Valori più alti sono stati osservati per tazze con un rivestimento posteriore costituito da perline e dimensioni dei pori di circa 250 μm, come Pinnacle Porocoat. Mentre ci sono chiare differenze nella struttura porosa dei due gruppi analizzati nel nostro studio, è da notare che abbiamo visto prove di un buon attaccamento osseo su entrambi i disegni.
Ad oggi, i componenti acetabolari stampati in 3D sono stati utilizzati principalmente in interventi di revisione e ri-revisione in cui la qualità ossea del paziente non è buona come in un’operazione primaria standard la cui causa è l’artrosi [ 1 , 6 ]. Ciò è probabilmente dovuto alla maggiore porosità e presa iniziale fornite dalle coppe stampate in 3D. Non si può escludere che il numero di operazioni primarie che adottano le coppe stampate in 3D aumenterà, considerando l’età decrescente dei pazienti sottoposti a interventi chirurgici d’anca primari, insieme all’aumento dell’invecchiamento della popolazione, che porta alla necessità di impianti più duraturi.
Un punto di forza di questo studio è stato l’uso dell’imaging micro-CT su impianti ortopedici che sono clinicamente utilizzati. Ho et al. [ 54 ] hanno riferito nel 2006 le capacità di questo metodo di indagine; da allora, diversi studi [ 19 , 20 , 21 , 35 , 55] hanno utilizzato la micro-TC per caratterizzare le proprietà morfometriche della struttura porosa di titanio (scaffold) stampata in 3D per potenziali applicazioni mediche, valutando anche i risultati biologici sia in vitro che in vivo. Tuttavia, siamo i primi a combinare l’analisi degli impianti stampati in 3D per l’applicazione clinica con le indagini micro-CT. Questo metodo ha fornito informazioni tridimensionali complete e non distruttive su forma, dimensioni e caratteristiche dei componenti prodotti, superando gli ostacoli riscontrati con campioni recuperati come la presenza di tessuto attaccato sulla superficie. Altre tecniche, come la microscopia, possono potenzialmente fornire dati simili ma limitati alla superficie esterna delle strutture, se il campione viene conservato o implicano una preparazione distruttiva per ottenere sezioni trasversali da analizzare [ 16, 26 ].
Una limitazione di questo studio è il piccolo numero di impianti. Solo i componenti prodotti da EBM sono stati considerati per il gruppo stampato in 3D, mentre un’altra tecnologia di produzione additiva (fusione laser selettiva, SLM) viene utilizzata anche per produrre questo tipo di coppe acetabolari. L’uso di impianti ortopedici stampati in 3D non è ancora molto diffuso, limitando quindi il numero di campioni disponibili per l’analisi. Tutti gli impianti analizzati sono stati recuperati dai pazienti; l’indagine sui recuperi rappresenta l’unico modo per analizzare in modo indipendente componenti di diversi produttori che hanno un discreto numero di campioni in analisi.
Conclusione
Questo è stato uno dei primi studi a caratterizzare le coppe acetabolari stampate in 3D, usando come riferimento componenti fabbricati in modo convenzionale. Abbiamo trovato differenze nelle strutture porose, con porosità e dimensioni dei pori maggiori osservate su tazze stampate in 3D. Sono state inoltre rilevate differenze morfologiche sulle superfici posteriori, legate ai diversi metodi di fabbricazione; sono necessarie ulteriori ricerche per comprendere meglio l’impatto clinico delle particelle parzialmente fuse sulla superficie degli impianti stampati in 3D.
Il lavoro futuro che coinvolge coorti di impianti più grandi ed eterogenei è necessario per capire se il passaggio a tecniche di stampa 3D per la produzione in serie di impianti ortopedici può fornire risultati sicuri e ben funzionanti.
Lo studio a questo indirizzo https://josr-online.biomedcentral.com/articles/10.1186/s13018-020-01665-y#Fig7