Gli impianti medici stampati in 3D sono in genere più rigidi e più forti del tessuto circostante e, sebbene non si adattino sempre bene agli stimoli biologici e fisici, tale rigidità è importante. I processi biologici dei nostri corpi sono naturalmente dinamici e molti ricercatori stanno lavorando per garantire che gli impianti stampati in 3D siano della massima qualità e funzionino bene all’interno del corpo umano .
I tessuti viventi si rimodellano costantemente in risposta ai cambiamenti. In particolare, i cambiamenti nella rigidità della matrice cellulare ed extracellulare (ECM) sono importanti per molti processi patologici e fisiologici, come la migrazione, la motilità cellulare e la differenziazione delle cellule staminali. Ma gli scienziati non comprendono appieno i fattori biomeccanici che sono strumentali allo sviluppo e alla manutenzione dei tessuti molli. Ecco perché sentiamo parlare così spesso di ingegneria dei tessuti – combinando cellule con scaffold, stampati in 3D o in altro modo, per fabbricare una sostituzione di tessuti autosufficiente.
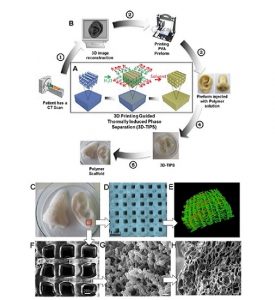 In un nuovo articolo, intitolato ” Scaffalature nanoibridi con memoria rigida generate da stampa 3D indiretta per impianti morbidi biologicamente sensibili “, un team collaborativo di ricercatori dell’Università del College di Londra , della Brunel University di Londra e del Royal Free London NHS Foundation Trust ha sviluppato il poli-urea termoresponsivo -uretano) (PUU) scaffold nanoibridi, con memoria di rigidità, utilizzando un metodo di separazione di fase termicamente indotto (3D-TIPS) guidato dalla stampa 3D.
In un nuovo articolo, intitolato ” Scaffalature nanoibridi con memoria rigida generate da stampa 3D indiretta per impianti morbidi biologicamente sensibili “, un team collaborativo di ricercatori dell’Università del College di Londra , della Brunel University di Londra e del Royal Free London NHS Foundation Trust ha sviluppato il poli-urea termoresponsivo -uretano) (PUU) scaffold nanoibridi, con memoria di rigidità, utilizzando un metodo di separazione di fase termicamente indotto (3D-TIPS) guidato dalla stampa 3D.
L’abstract dice: “La rigidità di cellule e tessuti è un importante parametro di segnalazione biomeccanica per i processi biologici dinamici; materiali polimerici reattivi che conferiscono funzionalità reattive sono quindi attraenti per in vivo impianti. Abbiamo sviluppato impalcati nanoibridi poli (urea-uretano) termoresponsivi con “memoria di rigidità” attraverso una versatile tecnica di separazione di fase indotta termicamente (3D-TIPS) guidata dalla stampa 3D. 3D-TIPS, una combinazione di stampa 3D con separazione di fase, consente separazione uniforme di fase e transizione di fase della soluzione polimerica su una grande interfaccia di rete all’interno della preforma sacrificale stampata, portando alla creazione di scaffold in scala completa con complesso anatomico su misura geometria. È stata prodotta una vasta gamma di proprietà meccaniche iperelastiche degli scaffold in elastomero morbido con pori interconnessi a porosità controllata e cristallinità multi-scala, non precedentemente ottenibili tramite tecniche di stampa diretta o separazione di fase da sole. coltura cellulare in vitro con modifiche minime alla forma. Questa ‘memoria di rigidità’ fornisce un supporto meccanico iniziale ai tessuti circostanti prima di graduale ammorbidimento per una migliore corrispondenza meccanica, aumentando le speranze per impianti morbidi personalizzati e biologicamente sensibili che promuovono la crescita delle cellule dei fibroblasti umani come modello e potenziale integrazione del tessuto scaffold. ”
Schema che delinea la separazione di fase controllata da micro-canali degli scaffold PUU-POSS 3D con struttura porosa interconnessa gerarchica.
Mentre il modulo elastico controllato di diversi materiali polimerici reattivi per l’ingegneria tissutale sono stati usati come modello per studiare effetti di rigidità in colture cellulari, il loro effetto di accoppiamento combinato di elasticità e cambiamento strutturale molecolare non ha una vasta gamma di rigidità regolabile. Ma i copolimeri a blocchi, come gli elastomeri poliuretanici (PU), hanno molte proprietà sintonizzabili senza dover cambiare la loro struttura molecolare – il metodo di auto-assemblaggio deve solo essere acceso. Se utilizzato in dispositivi cardiovascolari impiantabili a lungo termine, la PUU ha già dimostrato un’eccellente biocompatibilità, biostabilità, conformità e resistenza alla fatica, e alcune PU hanno anche memoria di forma.
Utilizzando materiali che rispondono agli stimoli, è possibile stampare strutture 3D dinamiche in grado di trasformare le loro forme o comportamenti, come la rigidità.
“Questo lavoro ha contribuito allo sviluppo di una serie di scaffold in elastomero nanoibrido termoresponsivo, con rigidità regolabile e struttura porosa interconnesso gerarchicamente, prodotto da una versatile tecnica di stampa 3D indiretta”, hanno scritto i ricercatori. “Per la prima volta, è stato osservato che la memoria di rigidità dello scaffold era guidata dalla transizione di fase e da un autoassemblaggio inverso da una fase semicristallina a una fase di gomma nanostrutturata quasi casuale. Le prime informazioni sulla risposta cellulare durante il rilassamento della rigidità degli scaffold in vitro sono promettenti per impianti morbidi biologicamente sensibili personalizzati. ”
Il team ha utilizzato AutoCAD 2014 per progettare preforme di alcool polivinilico 3D (PVA) per la produzione e la caratterizzazione di scaffold PUU-POSS, prima di esportare i file STL nel software Slic3r, “dove sono stati suddivisi in una serie di strati 200μm consecutivi” per versatile , stampa indiretta 3D-TIPS conveniente.
I ricercatori hanno scritto: “Le immagini ricostruite di file .stl digitali di un orecchio e di un naso sono state ottenute da immagini di scansione CT, tagliate con densità di riempimento del 50% e stampate come preforme PVA. La soluzione PUU-POSS è stata iniettata in ogni preforma e la preforma lavata come descritto per i gruppi RTC + H sopra, per produrre scaffold polimerici di forma anatomica. ”
Transizioni di fase, struttura cristallina, distribuzione delle dimensioni dei pori, morfologia e proprietà meccaniche degli scaffold PUU-POSS 3D (densità di riempimento del 50%) con temperature di lavorazione variabili.
Il team ha utilizzato la sua tecnica di stampa indiretta 3D-TIPS per fabbricare uno scaffold per tessuti resistente alla temperatura corporea, realizzato su una soluzione di elastomero nanoibrido PUU-POSS, che è stato confinato all’interno di una rete preformata PVA scalabile, stampata in 3D. Il team ha prodotto scaffold 3D con dimensioni macroscopiche uniformi e identici e contenuto di polimero, ma variabili proprietà cellulari e biomeccaniche, mediante il controllo termico della coagulazione della soluzione PUU e la separazione micro-fase delle catene polimeriche all’interno della rete.
“La proprietà più intrigante di questi scaffold, quella della ‘memoria della rigidità’, è guidata dall’auto-assemblaggio inverso della transizione di fase della struttura cristallina ordinata 3D in nanostrutture quasi-casuali di segmenti morbidi e duri a temperatura corporea, che conferisce l’unicità e desiderabili proprietà meccaniche dinamiche di rilassamento della rigidità con cambiamento di forma impercettibile “, hanno spiegato i ricercatori. “Il piccolo volume cambia, a causa del rilassamento della catena di imballaggio ordinata al punto di fusione dei segmenti molli all’interno della rete porosa interconnessa uniforme, contribuisce alla stabilità della forma dell’impalcatura con poca deformazione.”
Indipendentemente dalla rigidità iniziale in varie condizioni di processo termico, gli scaffold PUU-POSS realizzati con il metodo 3D-TIPS del team “ricordano” di rilassarsi nella loro fase di gomma iperelastica una volta raggiunta la temperatura di fusione dei segmenti molli.
“La tecnica 3D-TIPS apre l’uso di un’ampia gamma di polimeri biofunzionali e precedentemente non stampabili e dei loro nanocompositi e consente la sintonizzazione nell’architettura e nella rigidità di costrutti fabbricati non precedentemente ottenibili tramite tecniche di stampa diretta o separazione di fasi da solo”, ha concluso il team . “Il metodo è a basso costo con tempi brevi, anche per impianti intricati e personalizzati su misura per il paziente. Il potenziale per una migliore crescita cellulare e bio-reattività degli scaffold nel periodo postoperatorio di guarigione, a causa del rilassamento della rigidità, rappresenta una piattaforma tecnica promettente per lo sviluppo di impianti, dispositivi e robotica chirurgici responsivi ai tessuti biologici, con proprietà meccaniche dinamiche abbinate a soddisfare le linee cellulari dinamiche, i tessuti e gli organi. ”
Co-autori del giornale sono Linxiao wu, Jatinder Virdee, Elizabeth Maughan, Arnold Darbyshire, Gavin Jell, Marilena Loizidou, Mark Emberton, Peter Butler, Ashley Howkins, Alan Reynolds, Ian W. Boyd, Martin Birchall e Wenhui Song.