VR e stampa 3D per “riparare” il polmone: il lavoro del RI-MUHC tra ponti stampati e bioingegneria del tessuto
Il Research Institute of the McGill University Health Centre (RI-MUHC), a Montréal, sta sperimentando un approccio che combina realtà virtuale (VR) e stampa 3D per capire se, in futuro, alcune forme di danno polmonare possano essere riparate o “aggirate” con interventi mirati, riducendo i casi in cui l’unica opzione è il trapianto. L’idea di fondo è intervenire su porzioni specifiche dell’organo, invece di sostituirlo completamente, quando il danno è localizzato e quando rimangono aree di tessuto ancora funzionali.
Perché il polmone è un bersaglio difficile per il trapianto (e perché serve un’alternativa)
A differenza di altri organi, il polmone presenta criticità note: disponibilità limitata di donatori idonei, complessità chirurgica e risultati clinici che, in molti contesti, restano più delicati rispetto ad altri trapianti solidi. In parallelo, la prevalenza di patologie respiratorie tende a crescere con l’invecchiamento della popolazione e con l’esposizione a fattori ambientali. In questo quadro, un filone di ricerca che mira a “riparare invece di sostituire” prova a colmare un vuoto tra terapie mediche e trapianto.
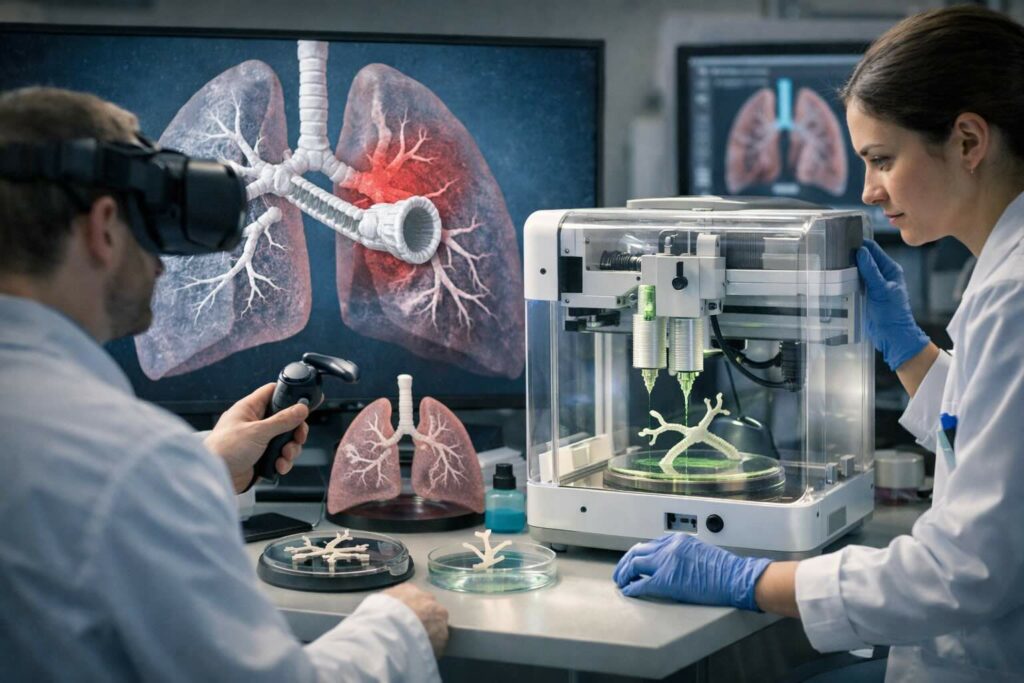
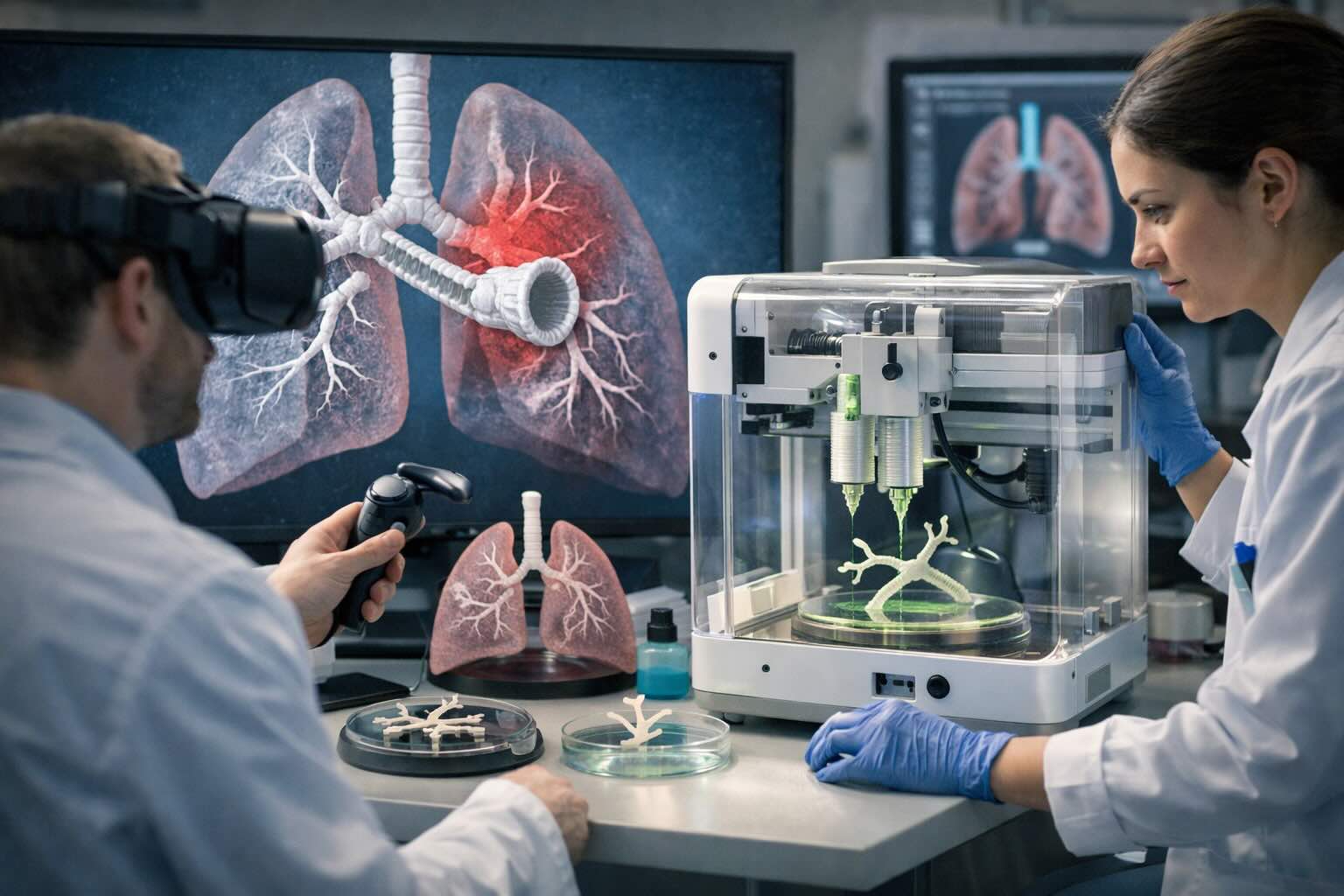
Come entra in gioco la VR: camminare “dentro” le vie aeree per localizzare il danno
Nel laboratorio del RI-MUHC, la VR viene utilizzata per esplorare modelli digitali tridimensionali dell’anatomia polmonare: i ricercatori possono muoversi lungo le vie aeree, osservare diramazioni e restringimenti, e individuare le aree compromesse. Lo scopo non è fare “visualizzazione”, ma supportare una pianificazione più concreta: decidere dove un intervento potrebbe creare un collegamento tra segmenti sani, bypassando porzioni non funzionanti.
L’idea dei “ponti” stampati: componenti cavi e ramificati per collegare aree sane
Il concetto descritto dal team guidato da Darcy Wagner (RI-MUHC) è quello di realizzare elementi strutturali cavi – una sorta di “bridge” – che possano connettere regioni respiratorie ancora valide, superando tessuto danneggiato o non ventilato correttamente. In questa prospettiva la stampa 3D non produce un “polmone completo”, ma componenti mirati con geometrie interne complesse (ramificazioni, curve, canali) che sarebbero difficili da ottenere con metodi tradizionali.
Dalla fattibilità geometrica ai materiali: perché serve un bioinchiostro specifico per il polmone
Un passaggio centrale riguarda i materiali. Per arrivare a strutture utilizzabili in un contesto biologico non basta “stampare la forma”: servono formulazioni compatibili con i tessuti e con la fisiologia polmonare. Nel racconto divulgativo legato al progetto, i test iniziali puntavano a dimostrare che si potessero stampare geometrie interne difficili (forme cave e ramificate) e, in seguito, a mettere a punto “inchiostri” adatti allo specifico ambiente del polmone, con caratteristiche diverse da quelle utili per altri distretti (per esempio cute o cuore).
Il limite di scala: l’ostacolo dei micro-dettagli e la strategia “guida + rigenerazione”
Un vincolo tecnico rimane la scala: alcune strutture coinvolte nello scambio gassoso hanno dimensioni dell’ordine del micrometro, oltre ciò che molte tecnologie di stampa possono riprodurre con fedeltà. Per questo la strategia descritta tende a concentrarsi su strutture più grandi che fungano da “guida” o supporto, lasciando che siano cellule e processi biologici a completare nel tempo parte dell’architettura fine dopo l’impianto, se e quando l’approccio arriverà a fasi applicative più avanzate.
A che punto è la ricerca: fase preclinica e prove di integrazione vascolare
Il lavoro è ancora descritto come preclinico. In questa fase, uno dei nodi è capire se i tessuti del ricevente possano integrare l’impianto e “colonizzare” la struttura, inclusa la componente vascolare, che è fondamentale per qualsiasi tessuto che debba restare vitale e funzionale. I passaggi verso la sperimentazione sull’uomo richiederebbero percorsi lunghi: sicurezza, stabilità dei materiali, standardizzazione del processo e prove robuste di efficacia.
Il contesto più ampio: biostampa e modelli polmonari, tra laboratorio e medicina rigenerativa
Parallelamente a questi “ponti” stampati, la ricerca internazionale sulla biofabbricazione polmonare lavora su due filoni complementari: (1) modelli in vitro più realistici per studiare malattie e testare terapie; (2) tecniche di rigenerazione e bioingegneria che, nel lungo periodo, potrebbero supportare riparazioni tissutali o innesti. Il programma della Canada Excellence Research Chair in Lung Regenerative Medicine associato a Darcy Wagner, per esempio, cita lo sviluppo di nuove tecniche di manifattura basate su 3D bioprinting e componenti microfluidici per aumentare la precisione con cui generare tessuto polmonare e modelli ex vivo più funzionali.
Dalla ricerca alla comunicazione pubblica: cosa è stato mostrato dai media canadesi
Una parte delle informazioni che ha portato la notizia all’attenzione internazionale arriva da servizi giornalistici in Canada, che mostrano il lavoro in laboratorio (VR per esplorare la struttura, stampa di componenti e sviluppo di tessuti). In queste ricostruzioni si parla anche di biostampa per creare tessuto polmonare con materiali che gelificano dopo l’estrusione, un dettaglio utile per capire che l’approccio si colloca tra stampa di forme e ingegneria di materiali/tessuti, non nella semplice prototipazione plastica.