Nanochon chiude un round Seed Prime II da 4,1 milioni di dollari per portare in clinica un impianto al ginocchio stampato in 3D
Un round “oversubscribed” e totale raccolto a 11,3 milioni
Nanochon, azienda di dispositivi ortopedici con base a Washington, D.C., ha comunicato il closing di un round “Seed Prime II” con impegni di capitale per 4,1 milioni di dollari, definito oversubscribed, che porta la raccolta complessiva a 11,3 milioni di dollari. Il round è guidato da cultivate(MD), con contributi citati da The University of Virginia (UVA) Seed Fund, WSGR e Wealthing VC Fund, oltre ad altri investitori (con una quota rilevante proveniente da investitori già presenti).
Che cos’è Chondrograft™ e quale problema clinico mira a coprire
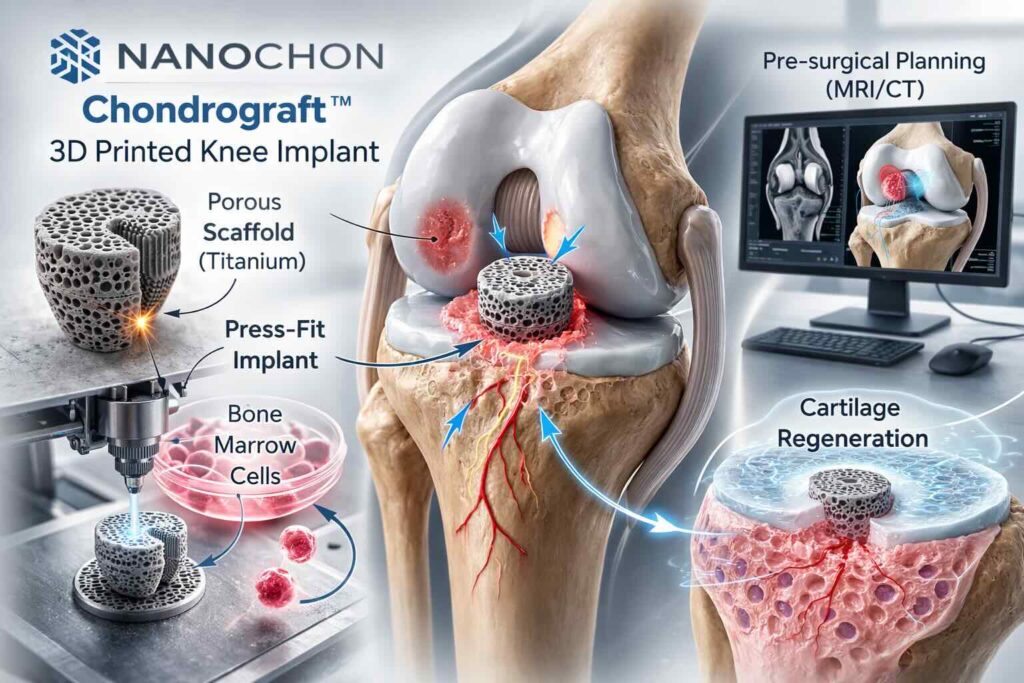
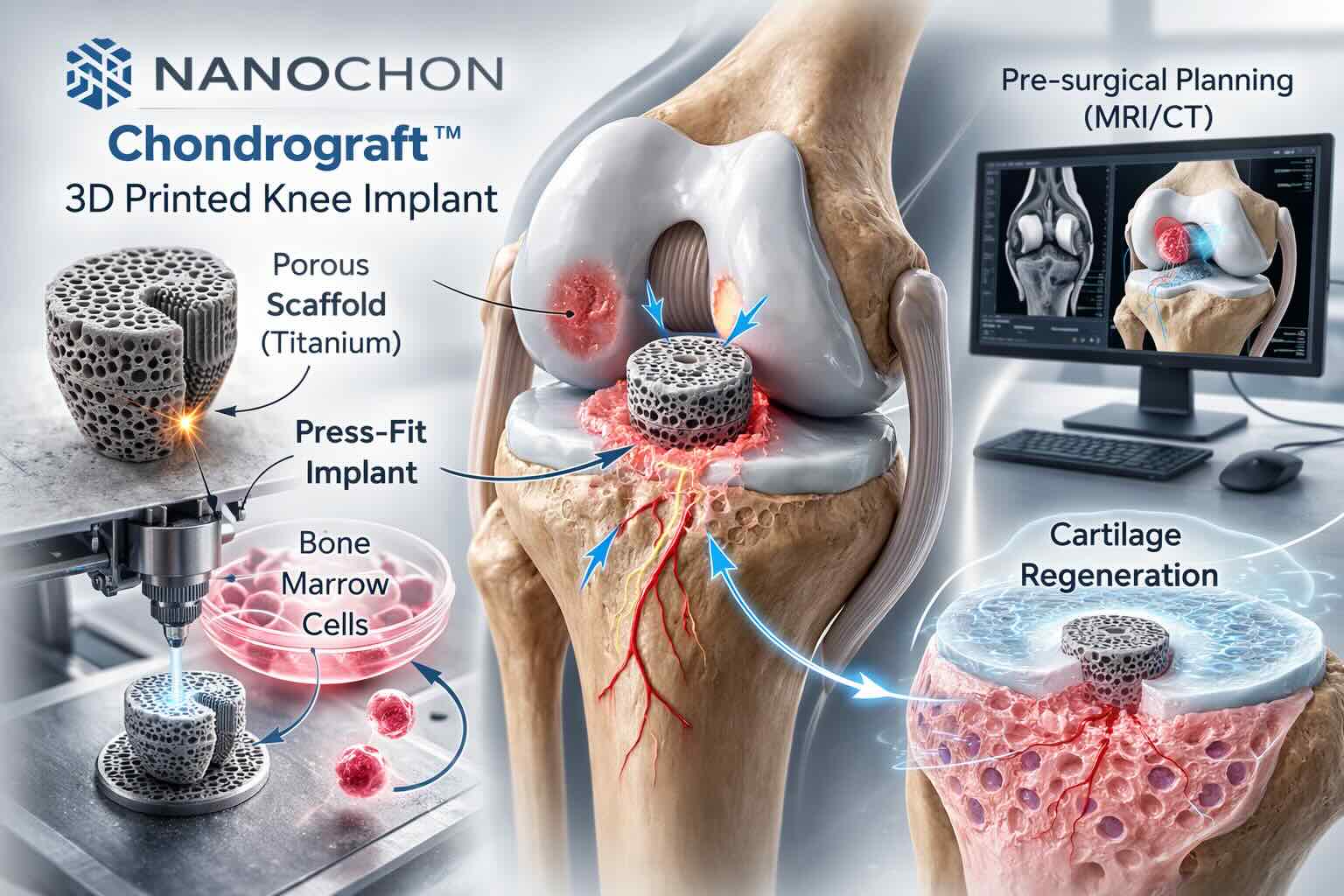
Il progetto principale di Nanochon è Chondrograft™, un impianto per trattare difetti focali della cartilagine articolare del ginocchio. L’idea dichiarata dall’azienda è intervenire su lesioni localizzate (“potholes” nella superficie cartilaginea), con un dispositivo che unisca funzione meccanica e ruolo di supporto biologico (scaffold), con l’obiettivo di favorire l’integrazione nel tempo con i tessuti circostanti.
Come si inserisce il dispositivo: press-fit e pianificazione pre-operatoria
Nanochon descrive un impianto progettato per un inserimento press-fit nell’area danneggiata, con un posizionamento mirato rispetto alla geometria del difetto. In parallelo, l’azienda dichiara una partnership con ProVoyance per sviluppare un software di pianificazione pre-operatoria basata su MRI, con l’obiettivo di standardizzare e supportare la preparazione dell’intervento (prima dell’ingresso in sala). ProVoyance, dal canto suo, si presenta come fornitore di piattaforme di pianificazione 3D che impiegano AI/ML per ricostruzioni ossee a partire da imaging (in particolare CT) e segnala esperienze in ambito software con clearance 510(k) in applicazioni ortopediche.
Dalla regolazione alla clinica: Canada come primo step
Nanochon ha impostato il primo percorso clinico in Canada: nel luglio 2025 l’azienda ha comunicato di aver ottenuto l’autorizzazione di Health Canada per avviare la prima sperimentazione first-in-human. Nel comunicato viene indicato come centro Durham Bone & Joint Specialists (DBJS) in Ontario, con Dr. Fathi Abuzgaya come Principal Investigator e un team di sub-investigators (tra cui Dr. Joel Lobo, Dr. Kajeandra Ravichandiran e Dr. Marcin Kowalczuk). L’impianto è dichiarato in valutazione in uno studio prospettico early feasibility su 10 pazienti (fascia 22–60 anni) con lesioni su femoral condyle e/o trochlea che abbiano fallito la terapia conservativa.
Perché la cartilagine è un “collo di bottiglia” clinico e cosa offre oggi lo standard of care
Le lesioni della cartilagine del ginocchio sono difficili da gestire perché la cartilagine articolare ha capacità rigenerative limitate e, quando il danno è focalizzato, le opzioni terapeutiche possono richiedere procedure e riabilitazioni impegnative. Nella pratica clinica esistono approcci come microfracture, trapianti osteocondrali (autograft/allograft) e tecniche cellulari come l’impianto di condrociti su matrice (ad esempio MACI). In questo contesto, la proposta di Nanochon si posiziona come dispositivo minimamente invasivo orientato a colmare un segmento di pazienti attivi con difetti focali, prima di soluzioni più “pesanti” come procedure ricostruttive complesse o, in fase degenerativa avanzata, l’artroplastica.
Uso dei fondi: studio first-in-human, R&D e preparazione della fase successiva
Nanochon dichiara che le risorse del round serviranno a sostenere lo studio first-in-human in Canada, approfondire le attività di R&D e preparare la pianificazione di uno studio pivotal più ampio. In un aggiornamento societario l’azienda indica anche l’intenzione di aprire un Series A da 20 milioni di dollari nel Q3 2026, funzionale a un trial nordamericano e alla preparazione del percorso verso autorizzazioni regolatorie negli Stati Uniti; nello stesso aggiornamento viene citato l’avvio dello studio di sicurezza first-in-human in British Columbia.
Nota regolatoria
Nanochon specifica che Chondrograft™ non è ancora approvato per la commercializzazione.