Rigenerazione ossea: possibilità e successo continui con il titanio nella produzione additiva
Nella rigenerazione ossea degli impianti di leghe di titanio prodotte dalla fusione laser a letto: una recensione , “gli autori esaminano il potenziale continuo del titanio nella bioprinting, poiché questo metallo continua a progredire nell’uso in campo medico. Sottolineando che in quest’area è stato svolto un “ampio lavoro”, gli autori impiegano tempo per individuare le aree aperte per il lavoro futuro, con particolare attenzione alla rigenerazione ossea.
Poiché il titanio è stato studiato in modo così approfondito e oggi è ampiamente utilizzato, gli autori sottolineano che non è un segreto che questi tipi di impianti metallici possano essere prodotti con successo nella stampa 3D e nella produzione additiva, con la fusione laser a letto (LPBF) che offre il maggiori benefici. I revisori sono interessati in particolare agli impianti Ti e Ti6Al4V e ai dettagli necessari per l’osteointegrazione.
La rigenerazione ossea si verifica attraverso il seguente:
Osteogenesi – formazione ossea.
Osteoinduzione – cellule mesenchimali indifferenziate vengono trasformate in osteoblasti; l’ectopico si forma in vivo.
Osteoconduzione – crescita ossea su matrici bio-inerte, consentendo una nuova colonizzazione cellulare.
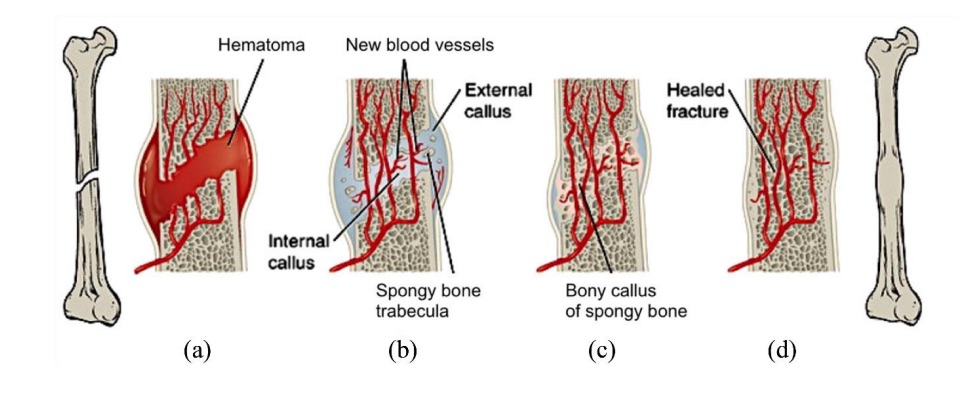
Anche il processo di guarigione ossea può essere esteso, a cominciare da un coagulo di sangue che si forma intorno alla frattura, quindi nuovi vasi sanguigni che si formano, nuova formazione ossea e quindi “la fase di rimodellamento”, che può richiedere anche anni. Per le leghe di titanio, i revisori sottolineano che la fabbricazione di una struttura porosa provoca una tale riduzione del modulo elastico che l’impianto diventa ancora più simile all’osso.
“Se questo non è il caso, l’effetto di schermatura dello stress provoca perdita ossea e allentamento dell’impianto e fallimento del processo”, affermano i ricercatori. “Oltre ad abbassare il modulo elastico, la natura porosa consente la crescita ossea nella struttura, rafforzando ulteriormente il legame tra l’impianto e l’osso esistente.”
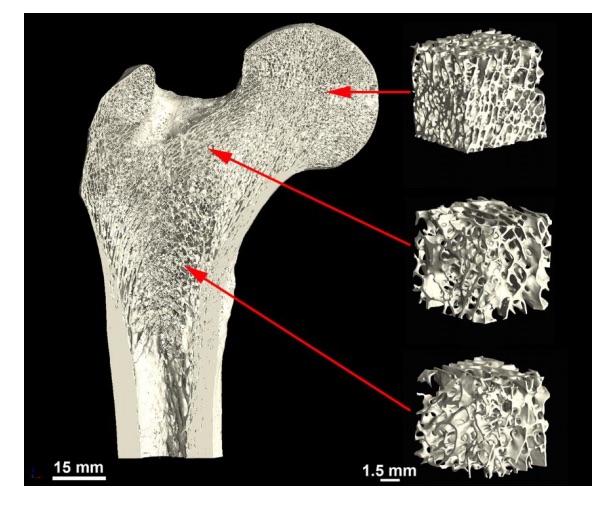
I nutrienti devono essere trasportati in aree in cui ci si aspetta che l’osso si sviluppi, e ci deve essere spazio sufficiente per la vascolarizzazione, con spazi porosi di dimensioni esatte.
Uno degli argomenti più interessanti riguarda l’analisi degli scaffold dei biomateriali, con una varietà di materiali diversi che promuovono la crescita delle ossa, come ad esempio:
Ceramica
metalli
polimeri
compositi
Ciascuno di questi diversi materiali può anche avere impatti diversi sulla rigenerazione ossea.
“Pertanto, approcci simili a tutti i materiali, porosità e dimensioni dei pori non possono essere suggeriti come guida generale. Anche gli impianti caricati / scaricati possono richiedere diversi vuoti in termini di volume e forma “, affermano i revisori.
Gli impianti richiedono quanto segue:
biocompatibilità
Topologia di superficie adatta
Proliferazione e differenziazione
Elevata porosità che fornisce crescita cellulare e trasporto di sostanze nutritive
Proprietà meccaniche affidabili
I campioni creati tramite LPBF possono mostrare un’ampia gamma di varianti a causa di strategie di costruzione, contorni, sporgenze e procedure di scansione. La produzione di reticoli porta sfide come i limiti di produzione, una miriade di possibili difetti e problemi di dimensioni.
L’adesione cellulare è suddivisa in tre diversi stadi, con l’attacco influenzato da fattori quali struttura superficiale, consistenza, bagnatura, composizione chimica e carica a pH fisiologico della superficie dell’impianto.
“Per gli studi in vitro, l’installazione di celle 3D sembra più preferibile in termini di valutazione della dimensione dei pori e della forma per la crescita delle ossa”, hanno concluso i revisori. “Per gli studi in vivo, le esigenze di osservazione a lungo termine con l’analisi non solo della crescita ossea nell’impianto, ma anche l’analisi delle ossa e dei tessuti circostanti”.