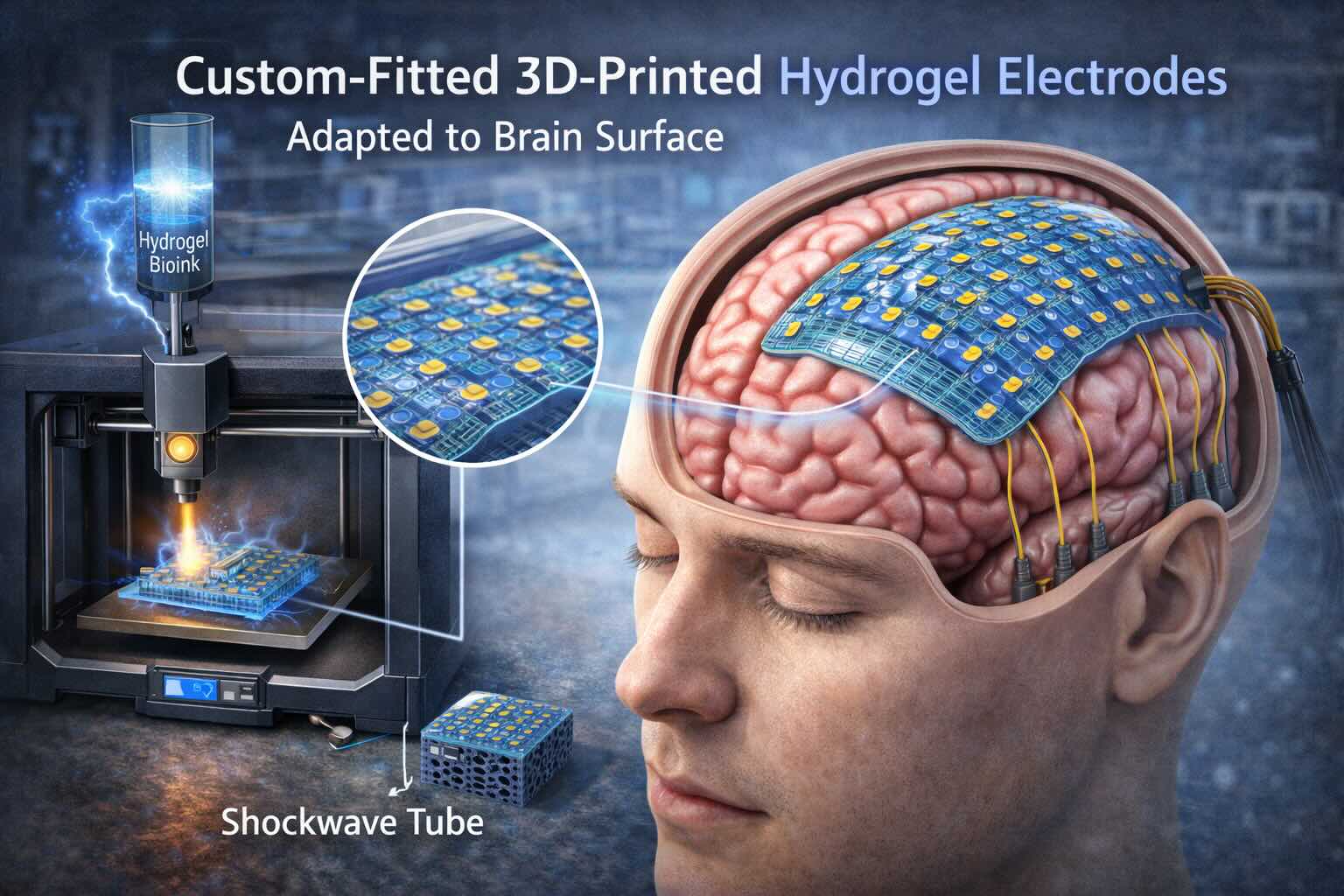
Un gruppo di ricercatori della Penn State University, guidato da Tao Zhou, Wormley Family Early Career Professor of Engineering Science and Mechanics, ha sviluppato un metodo per produrre elettrodi per il monitoraggio cerebrale stampati in 3D, capaci di adattarsi alla geometria individuale della superficie del cervello di ciascun paziente. I risultati sono stati pubblicati sulla rivista scientifica Advanced Materials e rappresentano un passo avanti significativo nel campo delle interfacce neurali morbide per il monitoraggio e la potenziale terapia delle malattie neurodegenerative.
Il problema delle interfacce neurali convenzionali
Le interfacce neurali sono dispositivi che entrano a contatto con la corteccia cerebrale per raccogliere segnali elettrici, monitorare l’attività neuronale o stimolare aree specifiche del cervello. Queste tecnologie trovano applicazione nel monitoraggio di patologie come l’epilessia, il morbo di Parkinson e l’Alzheimer, nonché nello sviluppo di protesi neurali e interfacce cervello-computer.
Il problema principale degli elettrodi tradizionali è che sono prodotti con materiali rigidi e in forme standardizzate, pensate per un cervello medio. In realtà, la struttura della corteccia cerebrale — con le sue circonvoluzioni chiamate giri e i suoi solchi denominati solci — varia sensibilmente da persona a persona in base a fattori come statura, peso, età e sesso. Un elettrodo rigido e non personalizzato non riesce a seguire queste irregolarità superficiali, il che si traduce in un contatto instabile con il tessuto, qualità del segnale ridotta e potenziale danno meccanico al tessuto cerebrale.
Come ha spiegato lo stesso Tao Zhou: “Nonostante questo, cerchiamo di adattare le interfacce neurali ai cervelli come se avessero tutti strutture identiche. Questo ci ha motivato a creare elettrodi su misura per ciascun individuo, basati sulla struttura del suo cervello.”
Dal modello MRI all’elettrodo su misura: il processo produttivo
Il processo sviluppato dalla Penn State University parte dalla risonanza magnetica (MRI) del paziente. I dati di imaging vengono elaborati attraverso un’analisi agli elementi finiti (Finite Element Analysis, FEA), una tecnica computazionale che consente di modellare il comportamento meccanico di strutture complesse. Questo approccio permette al team di generare un modello tridimensionale preciso della superficie corticale del paziente e, a partire da esso, di progettare un elettrodo geometricamente ottimizzato per quella specifica anatomia.
Una volta definita la forma, l’elettrodo viene prodotto tramite Direct Ink Printing (noto anche come Direct Ink Writing, DIW), una tecnica di stampa 3D a base di inchiostro che opera a temperatura ambiente depositando il materiale strato per strato attraverso un ugello. Questa tecnica, a differenza dei processi fotolitografici o delle tecnologie che richiedono camere bianche (clean room), non impone requisiti di infrastrutture specializzate, abbattendo i costi di produzione e i tempi di personalizzazione in modo sostanziale.
Il materiale: idrogel ad alto contenuto d’acqua
Il materiale base degli elettrodi è un idrogel, un polimero a rete tridimensionale che trattiene grandi quantità di acqua — in alcune formulazioni fino all’80-90% del peso totale. Questa composizione rende l’idrogel meccanicamente molto più simile al tessuto cerebrale rispetto ai metalli, al silicio o ai polimeri rigidi tradizionalmente usati nell’impiantistica neurale. La vicinanza di modulo elastico tra elettrodo e tessuto riduce le forze di taglio all’interfaccia, limitando la risposta infiammatoria a lungo termine.
Il gruppo di Tao Zhou lavora da anni su materiali idrogelosi conduttivi per applicazioni neurali. Un precedente studio, condotto in collaborazione con Xuanhe Zhao del MIT e pubblicato su Nature Materials nel 2023, aveva già mostrato come idrogel polimerici conduttivi potessero fungere da elettrodi morbidi per il cuore e il cervello, con prestazioni comparabili ai metalli ma con una biocompatibilità superiore. Tao Zhou era coautore di quel lavoro come ex dottorando del MIT, prima di assumere la cattedra alla Penn State University.
La geometria a nido d’ape: flessibilità senza perdita di resistenza
Una delle caratteristiche tecniche più rilevanti dello studio pubblicato su Advanced Materials è la scelta di una geometria ispirata al nido d’ape (honeycomb) per la struttura degli elettrodi. Anziché creare un film solido e continuo, il team ha progettato una reticola esagonale che consente all’elettrodo di deformarsi elasticamente e adattarsi alle curve della corteccia senza rompersi.
Come ha dichiarato Zhou, “La struttura a nido d’ape ci aiuta a ridurre significativamente la rigidità degli elettrodi, senza sacrificarne la resistenza meccanica. Inoltre, ci permette di ridurre il materiale complessivo utilizzato durante la fabbricazione, riducendo i tempi di produzione, i costi e l’impatto ambientale.”
Questa scelta geometrica ha anche implicazioni pratiche rilevanti: un elettrodo più morbido si deforma seguendo i movimenti del cervello (ad esempio durante le pulsazioni vascolari), mantenendo un contatto stabile con la superficie corticale nel tempo.
Test su 21 modelli cerebrali umani
Per validare la passgenauigkeit (precisione di adattamento) degli elettrodi, il team della Penn State University ha stampato in 3D modelli fisici dei cervelli di 21 soggetti umani diversi, ricavati dalle rispettive scansioni MRI. Su ciascun modello hanno poi applicato gli elettrodi sviluppati e misurato quantitativamente quanto bene questi riuscissero ad aderire alla superficie corticale nelle zone dei giri e dei solci, confrontando i risultati con gli approcci convenzionali non personalizzati.
Gli elettrodi in idrogel con geometria a nido d’ape hanno dimostrato una connettività elettrica quasi perfetta, ovvero un contatto stabile e continuo con la superficie del modello cerebrale, superiore a quello ottenibile con i design tradizionali. Questo si traduce direttamente in una qualità del segnale elettrico più elevata e in una riduzione del rumore, aspetto critico nelle applicazioni di elettrocorticografia (ECoG) per il monitoraggio di patologie come l’epilessia.
Risultati in vivo: 28 giorni senza risposta immunitaria
Oltre ai test meccanici su modelli fisici, la ricerca ha incluso esperimenti su modelli animali con un follow-up di 28 giorni. Gli elettrodi impiantati non hanno prodotto una risposta immunitaria misurabile né un declino delle prestazioni elettriche nel corso del periodo di osservazione. Sia la qualità della trasmissione del segnale sia l’accuratezza delle misurazioni sono rimaste stabili, indicando una buona biocompatibilità e una tenuta meccanica a lungo termine.
Questo dato è particolarmente importante nel contesto degli impianti neurali permanenti o semi-permanenti, dove la risposta infiammatoria del tessuto cerebrale intorno all’elettrodo è uno dei principali fattori che portano alla degradazione del segnale nel tempo, fino alla perdita funzionale del dispositivo.
Prospettive cliniche e sviluppi futuri
Il team della Penn State University ha dichiarato che il passo successivo consisterà nell’ottimizzare la geometria degli elettrodi per patologie specifiche e per ambienti clinici reali. Lo stesso Zhou ha espresso l’intenzione di lavorare direttamente con pazienti per verificare come questo approccio possa supportare il monitoraggio cerebrale e il trattamento delle malattie in contesti ospedalieri.
Il metodo di fabbricazione basato su stampa 3D con Direct Ink Printing rappresenta un potenziale vantaggio rispetto alle tecnologie clean room convenzionali anche dal punto di vista economico e della scalabilità: produrre elettrodi personalizzati per ciascun paziente non richiederebbe più infrastrutture dedicate e costose, rendendo la tecnologia potenzialmente accessibile a un numero più ampio di centri di neurologia clinica.
In parallelo, il gruppo di ricerca di Tao Zhou aveva già esplorato nel 2025 applicazioni EEG non invasive con un elettrodo sottile simile a un capello, stampato in 3D e dotato di un inchiostro bio-adesivo, capace di monitorare l’attività cerebrale a lungo termine senza necessità di gel conduttivi tradizionali. La ricerca pubblicata su Advanced Materials nel 2026 estende questo percorso verso applicazioni impiantabili e personalizzate.
Il contesto della ricerca sugli elettrodi neurali morbidi e stampati in 3D
La ricerca della Penn State University si inserisce in un filone più ampio di studi sull’elettronica neurale morbida e stampata in 3D. La Carnegie Mellon University aveva in precedenza sviluppato l’array CMU, un microelettrodo prodotto con stampa 3D Aerosol Jet per interfacce cervello-computer, pubblicato su Science Advances. Il MIT, attraverso il gruppo di Xuanhe Zhao e la startup SanaHeal, aveva dimostrato la possibilità di usare idrogel polimerici conduttivi come elettrodi per cuore, cervello e altri organi. La rivista scientifica Advanced Materials aveva già pubblicato nel 2026 il contributo della Penn State University, con il titolo “3D-Printable, Honeycomb-Inspired Tissue-Like Bioelectrodes for Individualized Gyral Patterns”.
Questi sviluppi indicano una tendenza chiara nel settore: sostituire i materiali rigidi e standardizzati degli impianti neurali con strutture morbide, biocompatibili e su misura, prodotte tramite tecnologie di stampa 3D accessibili e scalabili.