I ricercatori del Texas A&M realizzano bioink “NICE” per creare tessuti ossei funzionali
La gestione dei difetti ossei e delle lesioni mediante trattamenti tradizionali può essere lenta e costosa. Quando le ossa si rompono, le cellule ossee di solito possono ripararle, a meno che la rottura non sia troppo grande. In quel caso, i clinici si sono storicamente trasformati in innesti ossei utilizzando segmenti di osso non essenziali prelevati da altre parti dello stesso paziente; l’osso dei fianchi, del bacino, del mento o delle costole può fare il lavoro. Sfortunatamente, ciò richiede ulteriori interventi chirurgici, che si traducono in più dolore per i pazienti e, fondamentalmente, esiste un limite alla quantità di chirurghi ossei non essenziali che possono assumere da un paziente.
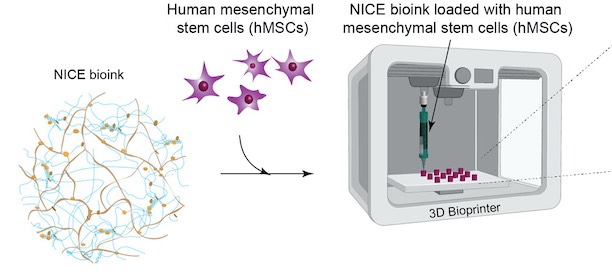
Come in molti campi, il bioprinting sta sconvolgendo il modo in cui gli specialisti della sanità pensano di risolvere i problemi. Quindi, con una stima di 500.000 procedure annuali di innesto osseo negli Stati Uniti e oltre 2 milioni in tutto il mondo, un efficace sostituto osseo potrebbe cambiare milioni di vite. Nel tentativo di fabbricare costrutti 3D impiantabili specifici per il paziente per la medicina rigenerativa, gli scienziati del Dipartimento di Ingegneria biomedica della Texas A&M University hanno sviluppato una nuova formulazione di bioink per la bioprinting ossea 3D chiamata NICE, che è l’abbreviazione di Nanoengineered Ionic – Covalent Entanglement, e hanno continuato a dimostrare che questo bioink può ricostruire con precisione grandi strutture ossee basate su scansioni TC ottenute da pazienti reali.
Guidato da Akhilesh K. Gaharwar, professore associato presso il Dipartimento di Ingegneria biomedica , il gruppo di ricerca ha sviluppato un bioink altamente stampabile come piattaforma per generare tessuti funzionali su scala anatomica. Il loro studio è stato recentemente pubblicato sulla rivista scientifica Applied Materials and Interfaces dell’American Chemical Society , per cui affermano che i bioink NICE consentono un controllo preciso sulla stampabilità, proprietà meccaniche e caratteristiche di degradazione, consentendo la fabbricazione 3D personalizzata di strutture meccanicamente resilienti e cellulari.
Il bioprinting richiede biomateriali carichi di cellule che possono fluire attraverso un ugello come un liquido, ma si solidificano non appena si depositano. Questo è il motivo per cui i bioink devono agire sia da portatori di cellule che da componenti strutturali, richiedendo che siano altamente stampabili fornendo al contempo un microambiente robusto e adatto alle cellule. Tuttavia, il gruppo di ricerca ha capito che molti bioink attuali mancano di biocompatibilità, stampabilità, stabilità strutturale e funzioni specifiche dei tessuti sufficienti per tradurre questa tecnologia in applicazioni precliniche e cliniche.
Per affrontare questo problema, Gaharwar e il suo team stanno conducendo sforzi nello sviluppo dei bioink NICE più avanzati, essenzialmente una combinazione di due approcci di rinforzo, entanglement ionico-covalente e nanorinforzo. In effetti, i ricercatori affermano che per progettare i bioink rinforzati NICE per la bioprinting dei tessuti osteogenici , il bioink deve essere altamente stampabile, meccanicamente forte, indurre differenziazione osteogenica ed essere biodegradabile. Tuttavia, la difficoltà di combinare questi requisiti in un unico bioink è stata un grande ostacolo nella bioprinting sin dal suo inizio. Quindi, combinando questi due distinti metodi di rinforzo, NICE diventa un bioink robusto e superiore fornendo al contempo un microambiente altamente idratato e adatto alle cellule per la bioprinting osseo.
Secondo Texas A&M Today, Gaharwar ha affermato che lo sviluppo di tessuti ossei sostitutivi potrebbe creare nuovi entusiasmanti trattamenti per i pazienti che soffrono di artrite, fratture ossee, infezioni dentali e difetti craniofacciali.
“Il prossimo traguardo nella bioprinting 3D è la maturazione dei costrutti bioprinted verso la generazione di tessuti funzionali”, ha affermato Gaharwar. “Il nostro studio dimostra che il bioink NICE sviluppato nel nostro laboratorio può essere utilizzato per progettare tessuti ossei funzionali 3D”.
I bioink NICE hanno tre componenti principali: gelatina metacrililica (GelMA) reticolabile covalentemente (GelMA), kappa-carragenina (kCA) ionicamente reticolabile e nanosilicati caricati elettrostaticamente (Laponite XLG, ottenuto da BYK Additives & Instruments).
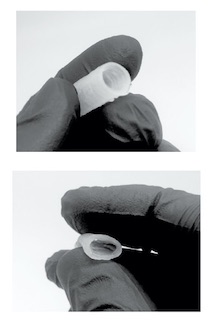
Per impalcature bioprint che possono dimostrare potenziali usi clinici, il team ha utilizzato i loro bioink osteoinduttivi NICE. Quindi le cellule staminali mesenchimali umane (hMSC) sono state incapsulate nel bioink NICE e bioprintate in scaffold 3D. Una volta completata la bioprinting, queste strutture NICE stampate in 3D cariche di cellule sono state reticolate per formare impalcature più forti. Questa tecnica ha permesso al laboratorio di produrre ricostruzioni su larga scala e compatibili con le cellule delle parti del corpo umano, inclusi orecchi, vasi sanguigni, cartilagine e persino segmenti ossei.
Subito dopo la bioprinting, le cellule chiuse iniziano a depositare nuove proteine ricche di una matrice extracellulare simile alla cartilagine che successivamente calcifica per formare un osso mineralizzato per un periodo di tre mesi. Texas A&M ha affermato che quasi il cinque percento di questi scaffold stampati era costituito da calcio, che è simile all’osso spugnoso, la rete di tessuto spugnoso che si trova tipicamente nelle ossa vertebrali.
Per capire come queste strutture bioprintate inducano la differenziazione delle cellule staminali, il team ha lavorato con Irtisha Singh del Texas A&M Health Science Center, che è stato co-investigatore, per utilizzare una tecnica di genomica di prossima generazione chiamata sequenziamento dell’intero transcriptome (RNA-seq) tecnologia, che cattura un’istantanea di tutte le comunicazioni genetiche all’interno della cellula in un dato momento.
Per quanto riguarda il bioprinting, i ricercatori hanno modificato un kit commerciale di stampanti 3D ANET A8 per utilizzare l’estrusione a vite. Hanno sostituito il gruppo estrusore in materiale termoplastico con un gruppo estrusore a vite stampato in 3D, che contiene un motore passo-passo, un binario di guida e un estrusore in argilla modificato.
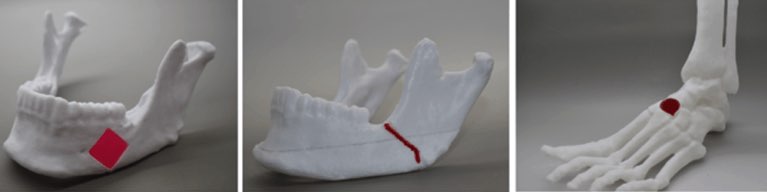
Per illustrare l’utilità pratica dei bioink NICE per la ricostruzione del tessuto osseo, il team ha dimostrato come creare impianti bioprinted su larga scala personalizzati per difetti craniofacciali su scansioni TC reali dei pazienti. Basandosi interamente su software open source, hanno utilizzato il software di modellazione 3D gratuito Meshmixer per elaborare i modelli e creare difetti ossei e le applicazioni di stampa 3D PrusaSlicer e Repetier Host per eseguire la bioprinting degli scaffold. Dopo la bioprinting, l’impalcatura è stata reticolata e impiantata in un modello termoplastico della mascella inferioreper dimostrare la vicinanza di adattamento. La forza di adattamento è stata inoltre dimostrata iniettando e reticolando il bioink NICE tra due sezioni di una frattura a tutto spessore per dimostrare che NICE è in grado di far aderire rapidamente le superfici insieme e resistere alle forze di taglio e delaminazione.
Finanziato dal New Innovator Award del Direttore del National Institutes of Health (NIH) , un premio della National Science Foundation (NSF) e un X-Grant della Texas A&M University, i ricercatori suggeriscono di aver scoperto un nuovo modo di progettare e produrre Tessuto osseo bioprintato 3D per favorire la rigenerazione ossea.
Inoltre, Gaharwar afferma di aver dimostrato che i bioink NICE altamente stampabili possono ricostruire con precisione grandi strutture ossee da scansioni TC ottenute da pazienti reali. Lo scopo della ricerca è consentire la bioprinting specifica per paziente di impalcature ossee per adattarsi esattamente alle loro lesioni. I ricercatori hanno dichiarato il loro desiderio di far sì che questa tecnica funga da personalizzazione e facile da lavorare con un’alternativa agli autotrapianti che fornirà ai chirurghi maggiori opzioni per la chirurgia ossea. E con l’obiettivo finale di ottenere la tecnologia del bioink NICE dal banco al capezzale, il team di Gaharwar prevede di stabilire la funzionalità in vivo del tessuto osseo bioprintato 3D.