Alcuni bioingegneri modellano le cellule per rendere pieghevoli le forme stampate in 3D dal tessuto vivente
I bioingegneri della UC San Francisco stanno utilizzando una tecnologia di modellazione cellulare 3D chiamata “assembly of cells” programmato dal DNA (DPAC) per stampare in 3D forme complesse di piegatura dal tessuto vivente. La ricerca potrebbe aiutare gli scienziati a creare tessuti sintetici complessi e funzionali.
 Il bioprinting in 3D ha già fatto molta strada consentendo agli scienziati di creare tessuti sintetici da cellule umane o animali. Ma anche i bioprinters più avanzati spesso non riescono a replicare con successo le caratteristiche strutturali chiave dei tessuti che crescono in base ai programmi di sviluppo. Le pieghe naturali nel tessuto umano, ad esempio, le numerose parti del nostro corpo che ci aiutano a funzionare, non sono facili da replicare con una stampante 3D.
Il bioprinting in 3D ha già fatto molta strada consentendo agli scienziati di creare tessuti sintetici da cellule umane o animali. Ma anche i bioprinters più avanzati spesso non riescono a replicare con successo le caratteristiche strutturali chiave dei tessuti che crescono in base ai programmi di sviluppo. Le pieghe naturali nel tessuto umano, ad esempio, le numerose parti del nostro corpo che ci aiutano a funzionare, non sono facili da replicare con una stampante 3D.
Una nuova ricerca condotta presso la UC San Francisco potrebbe segnare un’importante svolta nell’ingegneria dei tessuti, in particolare per quanto riguarda le strutture pieghevoli difficili da replicare. Gli scienziati dell’università hanno scoperto che modellando le cellule dei topi o le cellule umane – in particolare le cellule mesenchimali – a strati sottili di fibre della matrice extracellulare, sono in grado di creare ciotole, bobine e increspature dal tessuto vivente.
“Stiamo iniziando a vedere che è possibile abbattere i processi di sviluppo naturale in principi ingegneristici che possiamo quindi riutilizzare per costruire e capire i tessuti”, ha detto il primo autore Alex Hughes, un borsista postdottorato presso l’UCSF. “È un’angolazione totalmente nuova nell’ingegneria dei tessuti”.
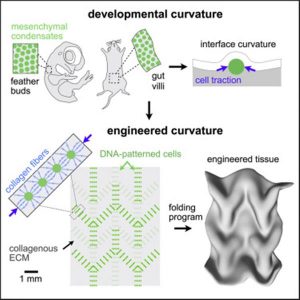
La ricerca prevede l’uso di una tecnologia di modellazione cellulare 3D chiamata assemblaggio di cellule programmato dal DNA, che può essere impiegata per impostare una sagoma spaziale di un tessuto. Questo modello di tessuto si ripiega poi in forme complesse, imitando il modo in cui i tessuti si assemblano gerarchicamente durante lo sviluppo.
Funziona perché le cellule mesenchimali “tirano” efficacemente sulla rete di fibre a matrice extracellulare (ECM) ropelike che le circondano, causando l’intera struttura ad arco o deformarsi.
Gli scienziati hanno già una solida comprensione su come programmare l’assemblaggio cellulare per manipolare il suo comportamento di piegamento. I ricercatori affermano che, organizzando in modo particolare le cellule mesenchimali, sono in grado di creare dei costrutti viventi che “modellano” in modi molto simili a ciò che i loro modelli semplici predicono.
“Lo sviluppo sta iniziando a diventare una tela per l’ingegneria, e rompendo la complessità dello sviluppo in principi ingegneristici più semplici, gli scienziati stanno iniziando a capire meglio e in definitiva a controllare la biologia fondamentale”, ha detto l’autore senior Zev Gartner, che ha descritto il nuovo processo come “un telaio fantastico per la costruzione di tessuti sintetici complessi e funzionali”.
Da qui, i ricercatori hanno diverse strade da esplorare. In primo luogo, vogliono scoprire se possono incorporare il programma di sviluppo del tessuto pieghevole in altri programmi che controllano la modellazione del tessuto, al fine di manipolare le cellule in modo completo. E in secondo luogo, vogliono dedicare più tempo a capire come le cellule si differenziano in risposta ai cambiamenti meccanici che si verificano durante la piegatura del tessuto in vivo.
In definitiva, questo importante lavoro potrebbe avere effetti a catena ovunque, da organi bioprintici in 3D o “organoidi” in miniatura per test antidroga, fino allo sviluppo di robot morbidi biologici.
“Mi ha stupito il modo in cui questa idea ha funzionato e il modo in cui le cellule si sono comportate”, ha aggiunto Gartner. “Questa idea ci ha mostrato che quando riveliamo solidi principi di progettazione evolutiva, ciò che possiamo fare con loro da una prospettiva ingegneristica è limitato solo dalla nostra immaginazione”.
Lo studio dei ricercatori, “Engineered Tissue Folding by Mechanical Compaction of the Mesenchyme”, è stato pubblicato sulla rivista Developmental Cell.