La stampa 3D applicata ai tessuti biologici sta entrando in una fase più matura: non si tratta più solo di depositare cellule vive in un gel, ma di organizzarle in strutture che assomiglino almeno in parte ai tessuti reali. È il caso del lavoro portato avanti dalla University of Oxford attraverso l’Oxford Martin Programme on 3D Printing for Brain Repair, un programma nato nel 2020 e concluso nel 2025 con l’obiettivo di capire se tessuti neurali stampati in 3D possano un giorno contribuire allo studio e alla riparazione del cervello.
Il tema va affrontato con prudenza. I ricercatori non hanno sviluppato una cura disponibile per pazienti con trauma cranico, ictus o malattie neurodegenerative. Hanno però dimostrato che è possibile costruire tessuti cerebrali umani più strutturati rispetto ai modelli cellulari tradizionali, con cellule organizzate in strati e capaci di mostrare segnali di interazione con tessuto ospite in modelli sperimentali.
Il problema: il cervello non è un semplice ammasso di cellule
Quando si parla di bioprinting, l’idea più immediata è quella di “stampare” un tessuto sostitutivo. Nel caso del cervello questa immagine è troppo semplice. La corteccia cerebrale ha un’organizzazione a strati, contiene diversi tipi di cellule e funziona grazie a connessioni estremamente precise. Non basta mettere insieme neuroni vivi: bisogna disporli nello spazio in modo coerente, mantenerli vitali, farli maturare e verificare se riescono a comunicare con il tessuto circostante.
Il programma Oxford Martin si è concentrato su questo punto: costruire tessuti neurali con un’architettura più controllata. I ricercatori hanno lavorato su cellule staminali pluripotenti indotte umane, cioè hiPSC, derivate da cellule umane riprogrammate. Queste cellule possono essere indirizzate verso diversi tipi cellulari, inclusi progenitori neurali destinati a formare componenti della corteccia cerebrale.
Una tecnica a gocce per costruire tessuto neurale
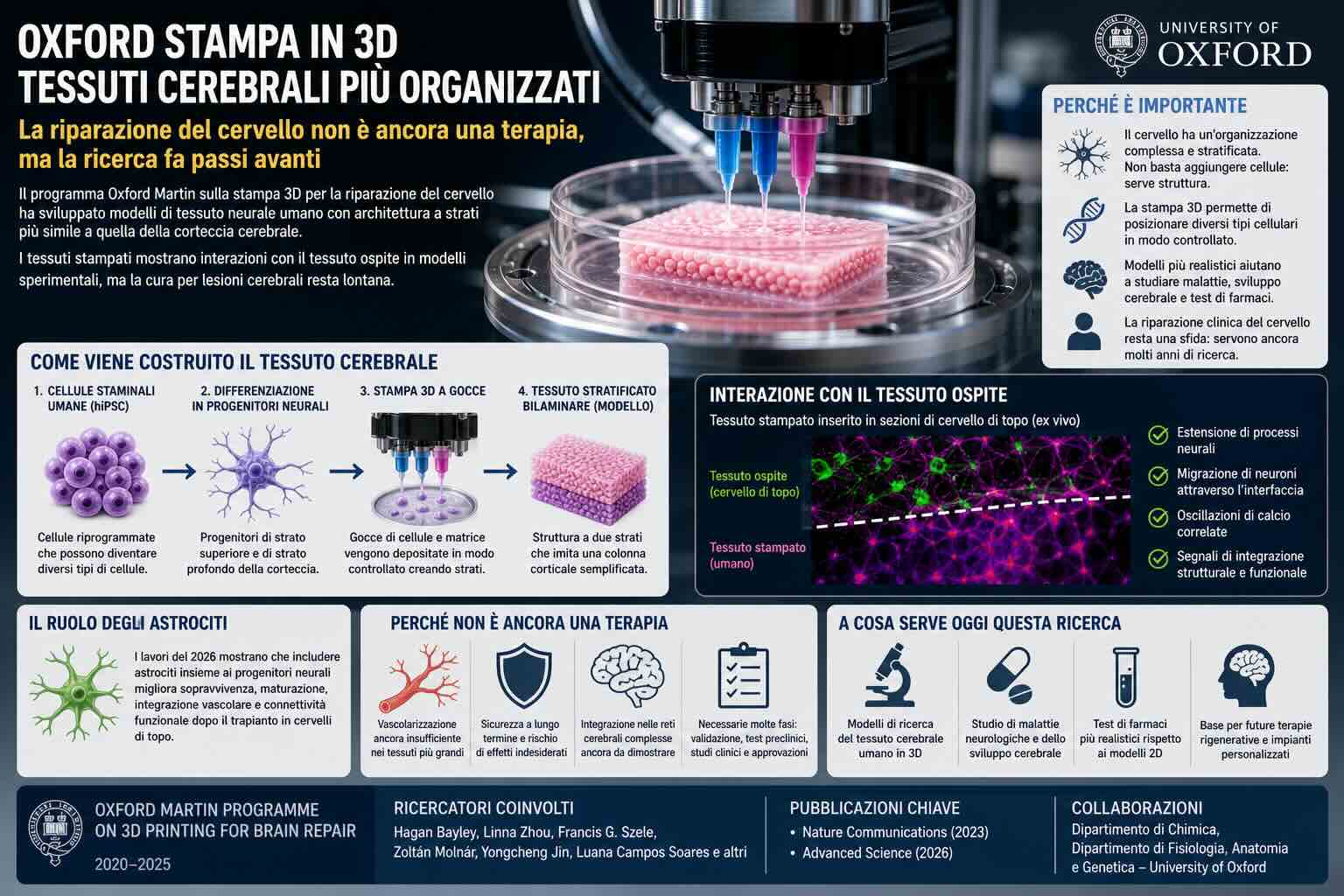
Il lavoro pubblicato su Nature Communications nel 2023 descrive una tecnica di stampa 3D a gocce. Invece di usare un approccio generico con cellule distribuite in modo casuale, il gruppo di Oxford ha differenziato cellule hiPSC in progenitori neurali associati a strati diversi della corteccia: progenitori di strato superiore e progenitori di strato profondo. Questi sono stati poi stampati in una struttura bilaminare, cioè composta da due strati, come modello semplificato di una colonna corticale.
La tecnica usa un sistema a gocce controllato da un attuatore piezoelettrico. Le gocce, contenenti cellule ed elementi di matrice extracellulare, vengono espulse in olio e organizzate secondo un disegno definito. Le gocce entrano in contatto e formano interfacce che permettono di creare reti tridimensionali morbide, senza affidarsi a uno scaffold rigido tradizionale.
Il risultato non è un cervello in miniatura e non è un impianto pronto. È un modello di tessuto corticale semplificato. Questo però rappresenta un passaggio importante per la ricerca: la struttura stampata mantiene per settimane una certa organizzazione a strati, esprime marcatori specifici e consente ai ricercatori di studiare come le cellule si muovono, maturano e stabiliscono connessioni.
Dalla stampa alla prova su tessuto cerebrale di topo
Nel lavoro del 2023, i tessuti corticali stampati sono stati inseriti in sezioni di cervello di topo mantenute vive in laboratorio, quindi in un modello ex vivo. Questo passaggio serve a osservare se le cellule umane stampate riescono a integrarsi strutturalmente con il tessuto ospite. I risultati hanno mostrato estensione di processi neurali, migrazione di neuroni attraverso il confine tra impianto e tessuto ospite e oscillazioni di calcio correlate tra le due aree, un segnale compatibile con interazione funzionale.
Questa parte va spiegata bene per evitare equivoci. Non significa che il tessuto stampato abbia riparato un cervello umano. Significa che, in un modello sperimentale controllato, le cellule stampate hanno mostrato comportamenti che i ricercatori cercano quando valutano l’integrazione tra impianto e tessuto nervoso. È una prova di principio, non una terapia clinica.
Perché la struttura conta più della semplice sopravvivenza cellulare
Uno dei limiti delle terapie cellulari per il sistema nervoso centrale è che le cellule possono sopravvivere poco, differenziarsi in modo non controllato o integrarsi male. Il cervello danneggiato è anche un ambiente difficile: infiammazione, cicatrici, mancanza di vascolarizzazione adeguata e segnali biochimici alterati possono compromettere l’attecchimento delle cellule trapiantate. Una review pubblicata su Frontiers in Bioengineering and Biotechnology nel 2026 sottolinea che la traduzione clinica delle terapie con cellule staminali neurali resta limitata proprio da sopravvivenza cellulare, differenziamento non controllato, integrazione del graft e microambiente post-lesione.
La stampa 3D può intervenire su una parte di questo problema: l’organizzazione. Se le cellule vengono posizionate in modo più simile al tessuto originario, possono avere migliori condizioni per maturare e stabilire connessioni. Ma la stampa 3D non risolve da sola vascolarizzazione, sicurezza, immunologia, controllo a lungo termine e recupero funzionale.
Il ruolo degli astrociti nella ricerca del 2026
Un altro passaggio del programma riguarda gli astrociti, cellule di supporto del sistema nervoso spesso meno note dei neuroni. Gli astrociti contribuiscono alla maturazione neuronale, alla formazione delle sinapsi, alla regolazione dell’attività nervosa e alla formazione dei vasi sanguigni. Nel 2026, la University of Oxford Medical Sciences Division ha descritto uno studio pubblicato su Advanced Science nel quale costrutti tridimensionali contenenti progenitori neuronali e astrociti hanno mostrato miglioramenti in sopravvivenza, maturazione, integrazione vascolare e connettività funzionale dopo trapianto in cervelli di topo.
Questo risultato sposta l’attenzione da “stampare neuroni” a “costruire un microambiente”. In un tessuto nervoso reale i neuroni non lavorano da soli: sono circondati da cellule gliali, vasi, matrice extracellulare e segnali chimici. Una strategia di bioprinting credibile dovrà quindi includere più tipi cellulari e non solo la componente neuronale.
A cosa serve oggi questa ricerca
Il primo impiego concreto non è l’impianto clinico nel paziente, ma la creazione di modelli più realistici per studiare il cervello umano. Tessuti neurali stampati con architettura controllata possono aiutare a comprendere lo sviluppo della corteccia, la risposta al danno, l’interazione tra tipi cellulari e l’effetto di farmaci o nutrienti che favoriscono l’integrazione. La stessa pubblicazione su Nature Communications indica tra le possibili applicazioni la valutazione di farmaci e sostanze capaci di promuovere l’integrazione del tessuto.
Questo aspetto è importante anche per l’industria farmaceutica. I modelli animali non riproducono sempre in modo fedele la biologia umana, mentre i modelli cellulari piatti in 2D sono troppo semplificati. Un tessuto 3D con diversi tipi cellulari e connessioni funzionali potrebbe diventare uno strumento più utile per studiare malattie neurologiche, testare molecole e osservare risposte cellulari in un ambiente più vicino al tessuto reale. Uno studio pubblicato su Cell Stem Cell ha mostrato che tessuti neurali umani assemblati tramite bioprinting possono formare circuiti funzionali tra sottotipi neurali definiti e diventare piattaforme per studiare reti neurali e test farmacologici.
Chi è coinvolto nel progetto
Il lavoro è accademico e multidisciplinare. Tra gli enti e gruppi coinvolti compaiono la University of Oxford, l’Oxford Martin School, il Department of Chemistry e il Department of Physiology, Anatomy and Genetics. Tra i nomi associati al programma e alle pubblicazioni figurano Hagan Bayley, Linna Zhou, Francis G. Szele, Zoltán Molnár, Yongcheng Jin, Luana Campos Soares e altri ricercatori dei gruppi coinvolti.
In questo caso non siamo davanti a una notizia guidata da un’azienda produttrice di stampanti 3D o da un prodotto commerciale. Il centro del lavoro è universitario: neuroscienze, biologia delle cellule staminali, microfluidica, bioingegneria e stampa 3D di tessuti molli.
Perché non siamo ancora alla riparazione del cervello
La distanza tra un tessuto neurale stampato in laboratorio e una terapia per il paziente è grande. Un impianto destinato al cervello dovrebbe sopravvivere nel tempo, collegarsi in modo sicuro alle reti esistenti, ricevere ossigeno e nutrienti, evitare crescita indesiderata, non generare tumori, non creare attività elettrica anomala e non peggiorare la lesione. Dovrebbe anche dimostrare un recupero funzionale misurabile, non solo integrazione cellulare.
La vascolarizzazione è uno dei nodi principali. Un tessuto più grande o più complesso non può vivere solo per diffusione passiva. Deve ricevere nutrienti e ossigeno in modo adeguato. Anche la maturazione è un ostacolo: molte cellule derivate da hiPSC possono richiedere settimane o mesi per acquisire caratteristiche più simili a quelle adulte. A questo si aggiungono i problemi di scala, ripetibilità e sicurezza regolatoria.
La differenza tra organoide, scaffold e tessuto stampato
Nel linguaggio comune tutti questi modelli vengono spesso messi insieme, ma non sono la stessa cosa. Gli organoidi cerebrali sono strutture cellulari tridimensionali che si auto-organizzano in coltura e possono imitare alcuni aspetti dello sviluppo del cervello. Gli scaffold sono supporti, spesso polimerici o idrogel, progettati per guidare la crescita cellulare. I tessuti biostampati cercano invece di posizionare cellule e materiali con un controllo spaziale più diretto.
Il vantaggio del bioprinting è proprio la possibilità di decidere dove collocare diversi tipi cellulari. Nel caso della corteccia cerebrale, questo controllo è utile perché il tessuto naturale è organizzato in strati. Il limite è che la complessità del cervello resta molto più alta di qualunque costrutto sperimentale oggi disponibile. La corteccia umana contiene più strati, molte sottopopolazioni cellulari, connessioni a lunga distanza e interazioni con vasi, cellule immunitarie e segnali biochimici.
Un possibile impatto sulla medicina personalizzata
L’uso di hiPSC apre anche una prospettiva legata alla personalizzazione. In teoria, cellule prelevate da un paziente potrebbero essere riprogrammate, differenziate in cellule neurali e usate per costruire tessuti compatibili con il profilo biologico della persona. Questo ridurrebbe il rischio di rigetto rispetto a cellule provenienti da donatori non compatibili. La University of Oxford sottolinea proprio questo vantaggio potenziale delle hiPSC nel contesto della riparazione tissutale.
Per ora, però, il percorso è di ricerca. Le cellule riprogrammate devono essere controllate con grande attenzione, perché la manipolazione cellulare porta con sé rischi biologici e regolatori. Prima di un uso clinico servono protocolli standardizzati, produzione in condizioni GMP, test di sicurezza, modelli animali più complessi, studi di efficacia e autorizzazioni da parte delle autorità sanitarie.
Un campo utile anche senza arrivare subito all’impianto
Anche se la riparazione clinica del cervello resta lontana, questi tessuti stampati possono avere valore già in laboratorio. Possono aiutare a studiare traumi cerebrali, malattie neurodegenerative, sviluppo della corteccia, comunicazione tra neuroni e glia, risposta a farmaci e meccanismi di integrazione tra tessuti. Il programma Oxford Martin, nella sua sintesi finale, indica che il controllo su tipi cellulari, struttura e ambiente potrà sostenere studi su trauma cranico, malattie neurodegenerative e sviluppo cerebrale umano.
In questo senso la stampa 3D non va vista solo come una tecnologia per “fare pezzi”, ma come uno strumento di biologia sperimentale. Permette di costruire modelli fisici nei quali geometria, posizione delle cellule e composizione del microambiente diventano variabili controllabili.
Scheda rapida
| Voce | Dettaglio |
|---|---|
| Progetto | Oxford Martin Programme on 3D Printing for Brain Repair |
| Ente principale | University of Oxford / Oxford Martin School |
| Periodo | 2020-2025 |
| Obiettivo | Studiare tessuti neurali stampati in 3D per modelli di cervello e possibili applicazioni future nella riparazione cerebrale |
| Tecnologia | Stampa 3D a gocce, microfluidica, bioink cellulari |
| Cellule usate | Cellule staminali pluripotenti indotte umane, progenitori neurali, astrociti in studi successivi |
| Modello biologico | Tessuti corticali semplificati, anche bilaminari |
| Pubblicazioni chiave | Nature Communications 2023, Advanced Science 2026 |
| Applicazione più vicina | Modelli di ricerca, studio dello sviluppo e test di farmaci |
| Applicazione più lontana | Impianti personalizzati per riparazione cerebrale |
| Limite principale | Integrazione sicura, vascolarizzazione, maturazione, controllo funzionale e validazione clinica |
Una direzione da seguire con attenzione
Il lavoro di Oxford mostra che il bioprinting cerebrale sta passando da strutture cellulari poco organizzate a modelli più controllati, con strati, tipi cellulari distinti e segnali di interazione funzionale. Questo non significa che la stampa 3D possa riparare oggi una lesione cerebrale. Significa però che i ricercatori stanno imparando a costruire tessuti neurali più simili, per struttura e comportamento, ai tessuti che vogliono studiare.
La notizia è rilevante perché sposta la stampa 3D biologica verso una domanda più difficile: non solo “possiamo stampare cellule vive?”, ma “possiamo organizzarle in modo abbastanza preciso da imitare una funzione biologica?”. Nel caso del cervello, questa domanda resta aperta. Il programma di Oxford non la chiude, ma fornisce strumenti e risultati che renderanno il prossimo passaggio più misurabile.